
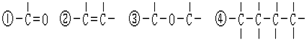
分析 (1)碳原子最多形成四个单键,氧原子最多形成两个;结构相似,在分子组成上相差一个或若干个CH2原子团的有机物互为同系物;
(2)甲烷是正四面体结构,四个氢原子完全等效;
(3)根据获取途径的能源消耗角度来分析.
解答 解:(1)根据碳的四价键结构、氧的二价键架构,结合该分子有支链,可知在CH3OC(CH3)3分子中必然存在的原子间连接形式有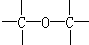 ;CH3OC(CH3)3 与CH3OCH2CH2CH3的结构相似,均只含有一个醚键,且分子组成上相差一个CH2原子团,故互为同系物.
;CH3OC(CH3)3 与CH3OCH2CH2CH3的结构相似,均只含有一个醚键,且分子组成上相差一个CH2原子团,故互为同系物.
故答案为:③;②
(2)天然气的主要成分是甲烷,根据分子式,可推测CH4的空间结构只有平面正方形和正四面体两种可能.若为平面正方形结构,则其二元取代物有两种同分异构体,而正四面体的二元取代物不存在同分异构体,故答案为:CH4;B;
(3)电解水消耗大量的电能,锌和硫酸反应也不符合工业上大量生产,只有利用太阳能使海水光解才是最经济的方法,
氢气储存和运输时容易爆炸,故答案为:③;贮存或运输.
点评 本题考查有机物结构和同系物、同分异构体的定义,难度不大,注意基础的掌握.


 名师点睛字词句段篇系列答案
名师点睛字词句段篇系列答案科目:高中化学 来源: 题型:选择题
| A. | R一定是非金属元素 | B. | R的最高价氧化物为R2O5 | ||
| C. | 最高价氧化物对应水化物H2RO4 | D. | R的气态氢化物为RH5 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol/LNaCl溶液含有nA个Na+ | |
| B. | 0.1molOH-含nA个电子 | |
| C. | 1molCu和足量稀硝酸反应产生nA个NO分子 | |
| D. | 常温常压下,22.4LCO2中含有nA个CO2分子 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
 在常温下,Fe 与水并不发生反应,但在高温下,Fe 与水蒸气可以发生反应,应用下列装置,在硬质玻璃管中放入还原铁粉和石棉绒的混合物,加热,并通入水蒸气,即可以完成高温下Fe 与水蒸气的反应实验.
在常温下,Fe 与水并不发生反应,但在高温下,Fe 与水蒸气可以发生反应,应用下列装置,在硬质玻璃管中放入还原铁粉和石棉绒的混合物,加热,并通入水蒸气,即可以完成高温下Fe 与水蒸气的反应实验.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | Na2CO3和HCl | B. | NaHSO4和Ba(OH)2 | C. | NaAlO2和H2SO4 | D. | AlCl3和NH3•H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铝热剂就是单指Fe2O3 粉和铝粉 | |
| B. | 检验从火星上带回来的红色物质是否是Fe2O3的操作步骤为:样品→粉碎→加水溶解→过滤→向滤液中滴加KSCN溶液 | |
| C. | 分别还原1mol Fe2O3所需H2、Al、CO 的物质的量之比3:2:3 | |
| D. | Fe2O3和Fe3O4都是具有磁性 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 该反应的方程式A+B?C | |
| B. | t1时刻反应达到平衡状态 | |
| C. | t2时刻,正反应速率大于逆反应速率 | |
| D. | 0~30min,用B表示该反应速率为0.03mol•L-1•min-1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com