
分析 有A、B、C、D四种无色溶液,它们分别是葡萄糖溶液、丙醇溶液、淀粉溶液、甲酸乙酯中的一种;
经实验可知:
①B、C均能发生银镜反应,说明B、C中都含有醛基,这几种物质中含有醛基的是葡萄糖和甲酸乙酯,所以B、C是葡萄糖和甲酸乙酯;
②A遇碘水变蓝色,淀粉遇碘试液变蓝色,所以A是淀粉溶液,则D是丙醇溶液;
③A、C均能发生水解反应,水解液均能发生银镜反应,能发生水解反应的是淀粉和甲酸乙酯,A是淀粉溶液,则C是甲酸乙酯,B是葡萄糖溶液,再结合题目分析解答.
解答 解:有A、B、C、D四种无色溶液,它们分别是葡萄糖溶液、丙醇溶液、淀粉溶液、甲酸乙酯中的一种;
经实验可知:
①B、C均能发生银镜反应,说明B、C中都含有醛基,这几种物质中含有醛基的是葡萄糖和甲酸乙酯,所以B、C是葡萄糖和甲酸乙酯;
②A遇碘水变蓝色,淀粉遇碘试液变蓝色,所以A是淀粉溶液,则D是丙醇溶液;
③A、C均能发生水解反应,水解液均能发生银镜反应,能发生水解反应的是淀粉和甲酸乙酯,A是淀粉溶液,则C是甲酸乙酯,B是葡萄糖溶液;
(1)通过以上分析知,A、B、C、D分别是淀粉溶液、葡萄糖溶液、甲酸乙酯、丙醇溶液,
故答案为:淀粉溶液;葡萄糖溶液;甲酸乙酯;丙醇溶液;
(2)①丙醇与氧气发生催化氧化,如果丙醇是1-丙醇,则催化氧化生成丙醛,如果是2-丙醇,则催化氧化生成丙酮,反应方程式为:2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CH2CHO+2H2O、2CH3CH(OH)CH3+O2$→_{△}^{Cu}$2CH3COCH3+2H2O,
故答案为:2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CH2CHO+2H2O、2CH3CH(OH)CH3+O2$→_{△}^{Cu}$2CH3COCH3+2H2O;
②甲酸乙酯水解生成甲酸和乙醇,水解方程式为:HCOOCH2CH3+H2O$?_{△}^{浓硫酸}$HCOOH+CH3CH2OH,
故答案为:HCOOCH2CH3+H2O$?_{△}^{浓硫酸}$HCOOH+CH3CH2OH.
点评 本题考查有机物推断,为高频考点,侧重考查学生分析推断能力,明确官能团及其性质关系是解本题关键,注意某些物质的特征反应,可以利用淀粉特性检验淀粉试液,题目难度不大.


科目:高中化学 来源: 题型:选择题
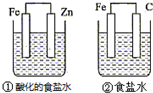
| A. | ①和②中铁的腐蚀均被加速 | |
| B. | ①和②中负极反应均是Fe-2e-═Fe2+ | |
| C. | ②中碳棒上反应是O2+2H2O+4e-═4OH- | |
| D. | ①装置中溶液pH会升高,②装置中溶液碱性增强 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 反应开始到10s,用Z表示的反应速率为0.158 mol•L-1•s-1 | |
| B. | 反应开始到10s,X的物质的量浓度减少了0.79 mol•L-1 | |
| C. | 反应开始到10s,Y的物质的量的减少是0.79mol | |
| D. | 反应的化学方程式为:X(g)+Y(g)?Z(g) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 一种新型乙醇电池用磺酸类质子作溶剂,比甲醇电池效率高出32倍.电池总反应为:C2H5OH+3O2═2CO2+3H2O,电池示意图如图.下面对这种电池的说法不正确的是( )
一种新型乙醇电池用磺酸类质子作溶剂,比甲醇电池效率高出32倍.电池总反应为:C2H5OH+3O2═2CO2+3H2O,电池示意图如图.下面对这种电池的说法不正确的是( )| A. | 该电池在工作时,溶液中的阳离子向正极移动 | |
| B. | 设每个电子所带电量为q库仑,NA表示阿伏加德罗常数,则46g乙醇被氧化产生12NAq库仑的电量 | |
| C. | 电池工作时电子由a极沿导线经灯泡再到b极 | |
| D. | 电池正极的电极反应式为:O2+4e-+2H2O═4OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①④ | B. | ②③ | C. | ③④ | D. | 全部 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | v(A)=0.5mol•L-1•s-1 | B. | v(B)=0.3mol•L-1•s-1 | ||
| C. | v(C)=0.8mol•L-1•s-1 | D. | v( D )=1.0mol•L-1•s-1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com