
ŌŚÅäÖĘŅ»¶ØĪļÖŹµÄĮæÅØ¶ČµÄNaOHČÜŅŗŹ±£¬ĻĀĮŠÄÄøöŌŅņ»įŌģ³ÉĖłÅäČÜŅŗÅضČĘ«øߣأ©
A£® ĖłÓĆNaOHŅŃ¾³±½ā
B£® ĻņČŻĮæĘæÖŠ¼ÓĖ®Ī“µ½æĢ¶ČĻß
C£® ÓŠÉŁĮæNaOHČÜŅŗ²ŠĮōŌŚÉÕ±Ąļ
D£® ¶ØČŻŹ±¹Ū²ģŅŗĆęŃöŹÓ
æ¼µć£ŗ ÅäÖĘŅ»¶ØČÜÖŹÖŹĮæ·ÖŹż”¢ĪļÖŹµÄĮæÅضČČÜŅŗµÄ·½·Ø£®
×ØĢā£ŗ »ÆѧŹµŃ黳±¾²Ł×÷£®
·ÖĪö£ŗ ·ÖĪö²Ł×÷¶Ōn”¢VµÄ¾ßĢåÓ°Ļģ£¬øł¾Żc=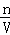 ·ÖĪö²»µ±²Ł×÷¶ŌÅØ¶ČµÄÓ°Ļģ£®
·ÖĪö²»µ±²Ł×÷¶ŌÅØ¶ČµÄÓ°Ļģ£®
½ā“š£ŗ ½ā£ŗA”¢ĖłÓĆNaOHŅŃ¾³±½ā£¬Źµ¼Ź³ĘĮæµÄĒāŃõ»ÆÄʵÄÖŹĮæ¼õŠ”£¬ĒāŃõ»ÆÄʵÄĪļÖŹµÄĮæ¼õŠ”£¬ĖłÅäČÜŅŗÅضČĘ«µĶ£¬¹ŹA“ķĪó£»
B”¢ĻņČŻĮæĘæÖŠ¼ÓĖ®Ī“µ½æĢ¶ČĻߣ¬ČÜŅŗĢå»żĘ«Š”£¬ĖłÅäČÜŅŗÅضČĘ«øߣ¬¹ŹBÕżČ·£»
C”¢ÓŠÉŁĮæNaOHČÜŅŗ²ŠĮōŌŚÉÕ±Ąļ£¬ŅĘČėČŻĮæĘæÄŚĒāŃõ»ÆÄʵÄĪļÖŹµÄĮæ¼õŠ”£¬ĖłÅäČÜŅŗÅضČĘ«µĶ£¬¹ŹC“ķĪó£»
D”¢¶ØČŻŹ±ŃöŹÓ¹Ū²ģŅŗĆę£¬Źµ¼Ź¼ÓĖ®Į泬¹żĮĖČŻĮæĘæµÄČŻ»ż£¬ĖłÅäČÜŅŗÅضČĘ«µĶ£¬¹ŹD“ķĪó£®
¹ŹŃ”£ŗB£®
µćĘĄ£ŗ æ¼²éŅ»¶ØĪļÖŹµÄĮæÅضČČÜŅŗÅäÖĘÓėĪó²ī·ÖĪö£¬øł¾Żc=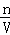 Ąķ½āČÜŅŗÅäÖĘµÄ²Ł×÷ÓėĪó²ī·ÖĪö£¬ÄŃ¶Č²»“ó£®
Ąķ½āČÜŅŗÅäÖĘµÄ²Ł×÷ÓėĪó²ī·ÖĪö£¬ÄŃ¶Č²»“ó£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ŌŚ±ź×¼×“æöĻĀ£¬ČōVL¼×ĶéÖŠŗ¬ÓŠµÄĒāŌ×ÓøöŹżĪŖn£¬Ōņ°¢·ü¼ÓµĀĀŽ³£ŹżæɱķŹ¾ĪŖ£Ø£©
A£® 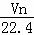 B£®
B£®  C£®
C£® 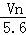 D£®
D£® 
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ŌŚŅ»¶ØĢõ¼žĻĀ£¬PbO2ÓėCr3+·“Ó¦£¬²śĪļŹĒCr2O72﹣ŗĶPb2+£¬ŌņÉś³É1molCr2O72﹣ ĖłŠčPbO2µÄĪļÖŹµÄĮæĪŖ£Ø£©
A£® 3.0mol B£® 1.5mol C£® 1.0mol D£® 0.75mol
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
Ć¾”¢ĀĮŗĻ½š3gÓė100mLĻ”H2SO4Ē”ŗĆĶźČ«·“Ó¦£¬½«·“Ó¦ŗóĖłµĆČÜŅŗÕōøÉ£¬µĆĪŽĖ®ĮņĖįŃĪ17.4g£¬ĒóĖćŌĮņĖįČÜŅŗµÄĪļÖŹµÄĮæÅØ¶Č£æ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ŅŃÖŖ1.505”Į1023øöXĘųĢå·Ö×ÓµÄÖŹĮæĪŖ8g£¬ŌņXĘųĢåµÄĦ¶ūÖŹĮæŹĒ£Ø£©
A£® 16g B£® 32g C£® 64g/mol D£® 32g/mol
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ijĶ¬Ń§°“ĻĀĮŠ²½ÖčÅäÖĘ500mL 0.20mol•L﹣1KClČÜŅŗ£¬Ēė»Ų“šÓŠ¹ŲĪŹĢā£®
ŹµŃé²½Öč ÓŠ¹ŲĪŹĢā
£Ø1£©¼ĘĖćĖłŠčKClµÄÖŹĮæ
ŠčŅŖKClµÄÖŹĮæĪŖ
£Ø2£©³ĘĮæ ¹ĢĢå ³ĘĮæ¹ż³ĢÖŠÖ÷ŅŖÓƵ½µÄŅĒĘ÷ŹĒ
£Ø3£©½«KCl¼ÓČė100mLÉÕ±ÖŠ£¬¼ÓŹŹĮæÕōĮóĖ®Čܽā ĪŖ¼ÓæģČܽā£¬æɲÉČ”µÄ“ėŹ©ŹĒ
£Ø4£©½«ÉÕ±ÖŠµÄČÜŅŗ×ŖŅĘÖĮ500mLČŻĮæĘæÖŠ ĪŖ·ĄÖ¹ČÜŅŗ½¦³ö£¬Ó¦øĆ²ÉČ”µÄ“ėŹ©ŹĒ
£Ø5£©ĻņČŻĮæĘæÖŠ¼ÓÕōĮóĖ®ÖĮæĢ¶ČĻß ŌŚ½ųŠŠ“Ė²Ł×÷Ź±Ó¦×¢ŅāµÄĪŹĢāŹĒ
ÄćČĻĪŖ°“ÉĻŹö²½ÖčÅäÖʵÄKClČÜŅŗµÄÅØ¶ČŹĒ·ńĪŖ0.200mol•L﹣1£¬ĒėĖµĆ÷ĄķÓÉ£® £®
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
Ēų±šSO2ŗĶCO2ĘųĢåæÉŃ”ÓƵķ½·ØŹĒ£Ø£©
A£® ĶØČėĘ·ŗģČÜŅŗÖŠ B£® ÓĆ“ų»šŠĒµÄľĢõ¼ģŃé
C£® ĶØČė³ĪĒåŹÆ»ŅĖ®ÖŠ D£® ĶØČėŹÆČļČÜŅŗÖŠ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĻĀĆęŹĒČĖĆĒ¶ŌÓŚ»ÆѧæĘѧµÄø÷ÖÖ³£¼ūČĻŹ¶£¬ĘäÖŠ“ķĪóµÄŹĒ£Ø£©
A£® »Æѧ½«ŌŚÄÜŌ“”¢×ŹŌ“µÄŗĻĄķæŖ·¢ŗĶ°²Č«Ó¦ÓĆ·½Ćę“óĻŌÉķŹÖ
B£® »ÆѧŹĒŌŚ±»ŌĖÓĆÓŚĘĘ»µ»·¾³¶ųƻӊÖĪĄķ»·¾³ĪŪČ¾
C£® »ÆѧŹĒŅ»ĆžßÓŠ¼«ĒæŹµÓĆŠŌµÄæĘѧ
D£® »ÆѧŹĒŅ»ĆÅŅŌŹµŃéĪŖ»ł“”µÄ×ŌČ»æĘѧ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
RĪŖ1”«18ŗÅŌŖĖŲ£¬ĘäŌ×ÓĖł¾ßÓŠµÄµē×Ó²ćŹżĪŖ×īĶā²ćµē×ÓŹżµÄ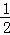 £¬ĖüæÉÄÜŠĪ³ÉµÄŗ¬ŃõĖįøłĄė×ÓÓŠ£ŗ¢ŁR2O42﹣£¬¢ŚRO42﹣£¬¢ŪR2O32﹣£¬¢ÜRO32﹣£¬ĻĀĮŠŠšŹöÅŠ¶ĻÕżČ·µÄŹĒ£Ø””””£©
£¬ĖüæÉÄÜŠĪ³ÉµÄŗ¬ŃõĖįøłĄė×ÓÓŠ£ŗ¢ŁR2O42﹣£¬¢ŚRO42﹣£¬¢ŪR2O32﹣£¬¢ÜRO32﹣£¬ĻĀĮŠŠšŹöÅŠ¶ĻÕżČ·µÄŹĒ£Ø””””£©
| ”” | A£® | µ±ĖüæÉŅŌŠĪ³É¢ŁŹ±£¬²»æÉÄÜŠĪ³É¢Ü |
| ”” | B£® | µ±ĖüæÉŅŌŠĪ³É¢ŚŹ±£¬æÉŅŌŠĪ³É¢ŪŗĶ¢Ü |
| ”” | C£® | µ±ĖüæÉŅŌŠĪ³É¢ŁŹ±£¬²»æÉÄÜŠĪ³É¢ŚŗĶ¢Ū |
| ”” | D£® | µ±ĖüŠĪ³É¢ŚŹ±£¬Ņ²æÉŅŌŠĪ³É¢Ł |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com