
| A. | 该反应过程的热效应称为燃烧热 | |
| B. | 该过程是吸热反应 | |
| C. | 生成物的总能量等于反应物的总能量 | |
| D. | 化学能转变成热能 |
分析 A、燃烧热是在101Kp时,1mol可燃物完全燃烧生成稳定的氧化物时所放出的能量,据此分析;
B、所有的燃烧均为放热反应;
C、化学反应一定伴随着热效应;
D、物质的燃烧有热量放出.
解答 解:A、燃烧热是在101Kp时,1mol可燃物完全燃烧生成稳定的氧化物时所放出的能量,而由于氢气的量不明确,故该过程放出的热量不一定是燃烧热,故A错误;
B、所有的燃烧均为放热反应,故氢气在氧气中的燃烧为放热反应,故B错误;
C、化学反应一定伴随着热效应,且此反应为放热反应,故此反应生成物的总能量小于反应物的总能量,故C错误;
D、物质的燃烧有热量放出,故此反应中化学能转变为热能,故D正确.
故选D.
点评 本题考查了物质的燃烧反应的热效应和反应物的能量和生成物的能量之间的关系,应注意的是燃烧均为放热反应.


科目:高中化学 来源: 题型:选择题
 如图,甲容器有一个移动活塞,能使弃器保持恒压.起始时向甲中充入2mol SO2、1mol O2,向乙中充入4mol SO2、2mol O2.甲、乙的体积都为1L(连通管体积忽略不计).保持相同温度和催化剂存在的条件下,关闭活塞K,使两容器中各自发生下述反应:2SO2(g)+O2(g)?2SO3(g).达平衡时,甲的体积为0.8L.下列说法正确的是( )
如图,甲容器有一个移动活塞,能使弃器保持恒压.起始时向甲中充入2mol SO2、1mol O2,向乙中充入4mol SO2、2mol O2.甲、乙的体积都为1L(连通管体积忽略不计).保持相同温度和催化剂存在的条件下,关闭活塞K,使两容器中各自发生下述反应:2SO2(g)+O2(g)?2SO3(g).达平衡时,甲的体积为0.8L.下列说法正确的是( )| A. | 乙容器中SO2的转化率小于60% | |
| B. | 平衡时SO3的体积分数:甲>乙 | |
| C. | 打开K后一段时间.再次达到平衡.甲的体积为1.4 L | |
| D. | 平衡后向甲中再充入2mol SO2、1mol O2.和3moLSO3,平衡向正反应方向移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | X>Z>Y>W | B. | Z>W>X>Y | C. | Z>X>Y>W | D. | Z>Y>X>W |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 溴化钙的化学式:CaBr | B. | 乙烯的结构简式:CH2CH2 | ||
| C. | 氟离子的结构示意图: | D. | 四氯化碳的电子式: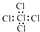 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
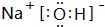 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铵盐化学性质都很稳定 | |
| B. | 锌片与稀硝酸反应可制得氢气 | |
| C. | 雷雨天气时空气中能生成少量的氮氧化物 | |
| D. | O2、NO、NO2都能用浓硫酸干燥,且通常情况下能共存 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原NaBr溶液分层,上层液体呈现橙色 | |
| B. | 原NaBr溶液分层,下层液体呈现橙色 | |
| C. | 原KI溶液分层,上层几乎无色 | |
| D. | 原KI溶液分层,下层呈现紫红色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | AlCl3溶液中加入足量的氨水:Al3++3OH-═Al(OH)3↓ | |
| B. | 用FeCl3溶液腐蚀印刷电路板:2Fe3++Cu═2Fe2++Cu2+ | |
| C. | 钠与水的反应:Na+H2O═Na++OH-+H2↑ | |
| D. | 氯气跟水反应:Cl2+H2O═2H++Cl-+ClO- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com