
| A. | 将胆矾加热除去结晶水后,称取32 g溶解在1 L水里 | |
| B. | 称取胆矾50 g,溶解在1 L水里 | |
| C. | 将32 g胆矾溶于水,然后将此溶液稀释至1 L | |
| D. | 将50 g胆矾溶于水,然后将此溶液稀释至1 L |
分析 1L 0.2mol•L-1的硫酸铜溶液中含有硫酸铜的物质的量为:0.2mol/L×1L=0.2mol,需要无水硫酸铜的质量为:160g/mol×0.2mol=32g,需要胆矾的质量为:250g/mol×0.2mol=50g,注意最终得到的溶液不等于加入水的体积,据此进行解答.
解答 解:1L 0.2mol•L-1的硫酸铜溶液中含有硫酸铜的物质的量为:0.2mol/L×1L=0.2mol,需要无水硫酸铜的质量为:160g/mol×0.2mol=32g,需要胆矾的质量为:250g/mol×0.2mol=50g,
A.32g无水硫酸铜的物质的量为0.2mol,0.2mol硫酸铜在1L水中所得溶液体积不是1L,故A错误;
B.50g胆矾为0.2mol,但溶解在1L水中,所得溶液体积不是1L,故B错误;
C.配制1L 0.2mol•L-1的硫酸铜溶液,需要胆矾的质量为50g,故C错误;
D.50g胆矾的物质的量为0.2mol,将0.2mol胆矾溶解后再将此溶液稀释至1 L,所得溶液浓度为0.2mol/L,满足条件,故D正确;
故选D.
点评 本题考查了配制一定物质的量浓度的溶液的方法,该题是中等难度的试题,试题基础性强,贴近高考,难易适中,注重灵活性,侧重对学生能力的培养和解题方法的指导和训练,有利于培养学生的逻辑思维能力和严谨的规范实验操作能力.


 特高级教师点拨系列答案
特高级教师点拨系列答案科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
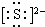 K+.
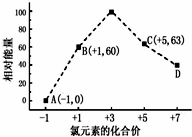
K+.| 离子半径 | 非金属性 | 酸性 | 沸点 |
| F+<D2- | A<B | D的最高价氧化物的水化物<E的最高价氧化物的水化物 | C的氢化物>E的氢化物 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
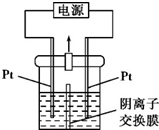 某实验小组的同学用图所示的实验装置进行电解反应,电解槽内装有KI-淀粉溶液,中间用阴离子交换膜隔开.在一定的电压下通电,发现左侧溶液变蓝色,一段时间后,蓝色逐渐变浅.
某实验小组的同学用图所示的实验装置进行电解反应,电解槽内装有KI-淀粉溶液,中间用阴离子交换膜隔开.在一定的电压下通电,发现左侧溶液变蓝色,一段时间后,蓝色逐渐变浅.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
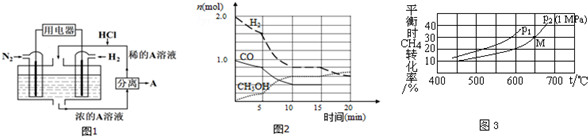
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
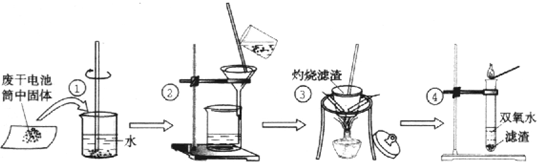
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com