
分析 (1)AlCl3属于强酸弱碱盐,在溶液中存在水解平衡,从平衡移动的角度分析;
(2)Fe3+易水解生成沉淀,可通过调节溶液pH的方法促进Fe3+的水解,注意不能引入新的杂质;
(3)纯碱溶液去油污的原理,碳酸根离子的水解显碱性,油脂在碱溶液中发生水解生成溶于水的高级脂肪酸盐和甘油容易洗去,碳酸钠溶液中碳酸根离子水解是吸热反应,升温促进水解,溶液碱性增强,去污效果好;
(4)根据平衡移动原理及溶度积解答,要使Mg (OH)2 固体进一步溶解,即平衡向右移动,可以加水,或降低Mg2+或OH-的浓度,加入与Mg2+或OH-反应的物质,以此解答该题.
解答 解:(1)Al2(SO4)3的水溶液中铝离子水解溶液显酸性,反应的离子方程式为:Al3++3H2O?Al(OH)3+3H+,氯化铝为强酸弱碱盐,Al3+发生水解,水解的方程式为Al3++3H2O?Al(OH)3+3H+,水解后溶液呈酸性,蒸干和灼烧过程中,HCl挥发,Al(OH)3不稳定,灼烧时分解生成Al2O3,
故答案为:酸;Al3++3H2O?Al(OH)3+3H+;Al2O3;
(2)FeCl3易水解生成氢氧化铁,加入Mg(OH)2粉末、MgO或MgCO3,调节溶液的pH,促进铁离子的水解,且不引入新的杂质,
故答案为:MgO或MgCO3;
(3)纯碱溶液去油污的原理,碳酸根离子的水解显碱性,反应的离子方程式为:CO32-+H2O?HCO3-+OH-,HCO3-+H2O?H2CO3+OH-,油脂在碱溶液中发生水解生成溶于水的高级脂肪酸盐和甘油容易洗去,碳酸钠溶液中碳酸根离子水解是吸热反应,升温促进水解,溶液碱性增强,去污效果好,
故答案为:CO32-+H2O?HCO3-+OH-,HCO3-+H2O?H2CO3+OH-,碳酸根离子水解是吸热反应,升温促进水解,溶液碱性增强,去污效果好;
(4)加入少量NH4Cl,NH4+与OH-结合生成氨水,故氢氧根的浓度减小,故平衡右移,通入HCl气体,氢氧根的浓度减小,故平衡右移,平衡正向移动,Mg(OH)2固体的质量减少,
故答案为:HCl或NH4Cl.
点评 本题考查了盐类水解、弱电解质电离平衡分析应用,水解平衡、电离平衡的影响因素分析判断,物质的分离和提纯,掌握物质性质和水解平衡、电离平衡的影响因素的分析是解题关键,铁离子易水解的性质用调节溶液pH的方法除杂,注意不能引入新的杂质,题目难度中等.


 通城学典默写能手系列答案
通城学典默写能手系列答案 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案科目:高中化学 来源: 题型:选择题
| A. | 某溶液中加入NaOH溶液,生成蓝色沉淀,说明原溶液中含有Cu2+ | |
| B. | 某溶液中加入BaCl2溶液,生成白色沉淀,说明原溶液中含有SO42- | |
| C. | 某溶液中加入硝酸银溶液,生成白色沉淀,说明原溶液中含有Cl- | |
| D. | 某溶液中加入稀硫酸,产生无色气体,将气体通入澄清石灰水中生成白色沉淀,说明原溶液中含有CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
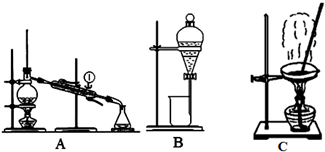
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 甲、乙、丙、丁四种物质中,甲、乙、丙均含有相同的某种元素,它们之间具有如图转化关系:(部分反应物,产物略去).下列有关物质的推断正确的是( )
甲、乙、丙、丁四种物质中,甲、乙、丙均含有相同的某种元素,它们之间具有如图转化关系:(部分反应物,产物略去).下列有关物质的推断正确的是( )| A. | 若甲为HNO3,则丁可能是Fe | B. | 若甲为AlCl3,则丁可能是氨水 | ||
| C. | 若甲为焦炭,则丁可能是SiO2 | D. | 若甲为NaOH 溶液,则丁可能是Cl2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向Na2S2O3溶液中通入足量氯气:S2O32-+2Cl2+3H2O═2SO32-+4Cl-+6H+ | |
| B. | 将磁性氧化铁溶于盐酸:Fe3O4+8H+═Fe3++2Fe2++4H2O | |
| C. | 将氯化亚铁溶液和稀硝酸混合:Fe2++4H++NO${\;}_{3}^{-}$═Fe3++2H2O+NO↑ | |
| D. | 铜溶于稀硝酸:3Cu+8H++2NO3-═3Cu2++2NO↑+4H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 德国化学家维勒首次实现了人工合成有机物 | |
| B. | 原子吸收光谱常用来确定物质中含有非金属元素 | |
| C. | 所有金属元素都可以用焰色反应来确定其存在 | |
| D. | SO2能溶于水,水溶液能导电,所以SO2是电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向盛有10mL水的量筒中倒入浓硫酸即得稀硫酸 | |
| B. | 向试管中滴加试剂时,将滴管下端紧靠试管内壁 | |
| C. | 使用试纸检验溶液的性质时,将试纸浸入溶液中 | |
| D. | 用托盘天平称量药品时,左盘放药品,右盘放砝码 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | M与A均能使酸性高锰酸钾溶液和溴水褪色 | |
| B. | B能发生消去、氧化、取代、缩聚等反应 | |
| C. | 1molM与足量烧碱溶液反应,可消耗2nmolNaOH | |
| D. | A、B、C各1mol分别与金属钠反应,放出气体的物质的量之比为1:2:2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com