
如图是某研究小组采用电解法处理石油炼制过程中产生的大量H2S废气的工艺流程。该方法对H2S的吸收率达99%以上,并可制取H2和S。下列说法正确的是
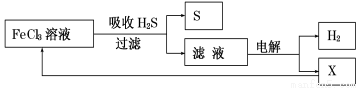
A.吸收H2S的离子方程式为:2Fe3++H2S =2Fe2++S↓+2H+
B.电解时选用阴离子交换膜,电解过程中的阳极区反应主要为:2Cl--2e- = Cl2
C.电解过程中若阴极产生2.24L气体,则阳极区产生0.2mol Fe3+
D.实验室可用点燃充分燃烧的方法消除H2S污染
科目:高中化学 来源:2015届浙江省高三上学期第二次质量检测化学试卷(解析版) 题型:选择题
下列各组物质的性质比较,正确的是
A.稳定性:H2O<NH3<PH3<SiH4
B.熔点:CO2<H2O<SiO2<KCl
C.酸性:HClO4>H3PO4>H2SO4>H2SiO3
D.粒子半径:K+>Na+>Mg2+>Al3+
查看答案和解析>>
科目:高中化学 来源:2015届浙江省高三上学期期中联考化学试卷(解析版) 题型:填空题
(每空2分,共12分)
PCl3与PCl5均是有机合成的重要中间体,两者存在以下相互转化关系:
PCl5(g)  PCl3(g) + Cl2(g) △H=a kJ·mol-1 在210℃时,将4mol PCl5气体充入
PCl3(g) + Cl2(g) △H=a kJ·mol-1 在210℃时,将4mol PCl5气体充入
2L真空密闭容器中发生上述反应,得到如下数据:
时间(s) | 0 | 20 | 40 | 60 |
n(PCl5) | 4 | 2.8 | 2 | 2 |
(1)已知上述反应在温度较高时才能自发进行,则a 0(填﹥、﹦、﹤);
(2)计算从20s至40s共20s的时间内,用PCl3表示的平均反应速率为 。210℃时该反应的平衡常数K值等于 。
(3)反应进行至60s后,将混合物的温度降低,重新达到平衡后氯气浓度将 (填“增大”、“减少”或“不变”)。
(4)欲增大该反应的K值,可采取的措施有(填序号)
A.降低温度 B.向混合气体中通入Cl2
C.使用高效催化剂 D.升高温度
(5)如右图是210℃时容器中PCl5物质的量的变化曲线,请在该图中补画出该反应在160℃时PCl5物质的量的变化曲线。

查看答案和解析>>
科目:高中化学 来源:2015届浙江省高三上学期期中联考化学试卷(解析版) 题型:选择题
设NA为阿伏加德罗常数的值。下列说法正确的是
A.常温常压下,17g羟基中含有的电子数目为10NA
B.常温常压下,28g由C2H4和C3H6组成的混合气体中含有的碳原子数目为2NA
C.0.05mol熔融的NaHSO4中含有的离子数目为0.15NA
D.标准状况下,6.72L NO2与水充分反应转移的电子数目为0.1NA
查看答案和解析>>
科目:高中化学 来源:2015届浙江省高三10月月考化学试卷(解析版) 题型:填空题
(本题包括2部分,共14分)
Ⅰ.(8分)X、Y、Z、W均为短周期元素组成的单质或化合物。在一定条件下有如下转化关系: X+Y→Z+W
(1)若构成X的阴、阳离子个数比为1︰2,且构成X的阴、阳离子中分别含有18个和10个电子,构成Z的阴、阳离子中均含有10个电子。则Z的电子式为 。
(2)若X、Y、Z、W四种物质均为分子,且X分子中含18个电子,Y、Z分子中均含有10个电子,单质W分子中含有16个电子。则此化学反应的类型为 。
(3)若X、W均为单质,Y、Z均为氧化物且Y、Z中氧的质量分数分别为50%和40%。则该反应的化学方程式为 。
(4)若X、Y、Z、W均为非金属氧化物,X的式量比Z的式量小16,Y的式量比W的式量大16,Y是光化学烟雾的主要“元凶”,则该反应的化学方程式为 。
Ⅱ.(6分)近年来,某些轻元素的含氢化合物及其复合体系作为氢源受到广泛关注。化合物A(XYH2)和B(XH)都是具有潜在应用价值的释氢材料。A受热分解生成固体化合物C并放出刺激性气体D,D可使湿润的pH试纸变蓝;B中X元素的质量分数为87.5%。A和B混合可优化放氢性能。研究发现,该混合体系的放氢反应分三步进行:(1)2A = C + D (2)D + B = A + H2 (3)C + B = E + H2
(5)X元素的名称为 。
(6)写出A和B混合放氢的化学反应方程式: 。
(7)A、C、E均能水解且生成同样的产物,请写出物质C与水反应的化学方程式: 。
查看答案和解析>>
科目:高中化学 来源:2015届浙江省高三10月月考化学试卷(解析版) 题型:选择题
根据“绿色化学”的思想,某化学家设计了下列化学反应步骤:
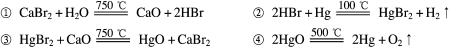
该方案的相关叙述正确的是
A.该实验的目的是制取HBr B.该过程的副产品是Hg
C.该过程得到的气体只有H2 D.该过程的本质是水的分解
查看答案和解析>>
科目:高中化学 来源:2015届浙江省高三10月月考化学试卷(解析版) 题型:选择题
己知X、Y、Z、W、N、U、V是短周期的主族元素,原子序数依次增大。X与N同主族,且与W都能形成A2B、A2B2型化合物;Z、W的单质常温下均为无色气体;Y原子的L层电子数是K层电子数的2倍;U原子的最外层电子数是其电子层数的2倍。下列说法不正确的是
A.N的单质的晶体属于金属晶体;U的氢化物的球棍模型示意图为
B.工业上V的单质的制备可以电解熔融的NV
C.Z的最高价氧化物对应的水化物能与其气态氢化物反应生成盐
D.X、Y、Z、W四种元素(按顺序)可组成原子个数比为5:1:1:3的化合物;也可形成结构式为X—W—Y ≡ Z的化合物
查看答案和解析>>
科目:高中化学 来源:2015届河南郑州市高三上第一次(10月)月考化学试卷(解析版) 题型:选择题
W、X、Y、Z均是短周期元素,X、Y处于同一周期,X、Z的最低价离子分别为 X2- 和
Z- ,Y+ 和Z- 离子具有相同的电子层结构。下列说法正确的是( )
A. 原子最外层电子数:X>Y>Z B. 单质沸点:X>Y>Z
C. 离子半径:X2->Y+>Z- D. 原子序数:X>Y>Z
查看答案和解析>>
科目:高中化学 来源:2015届河南省洛阳市高三上学期期中考试化学试卷(解析版) 题型:选择题
常温下,在下列给定条件的各溶液中,一定能大量共存的离子组是
A.1.0mol·L-1的HNO3溶液:NH4+、[Ag(NH3)2]+、Cl-、SO42-
B.c(H+)/c(OH-)=10-11的溶液:Na+、Ba2+、NO3-、Cl-
C.滴入酚酞显红色的溶液:Ca2+、Al3+、NO3-、HCO3-
D.滴入碘化钾淀粉溶液显蓝色的溶液:Na+、Fe2+、ClO-、SO42-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com