
 ��ͼ��ʾ�����ס�������װ�в�ͬ���ʵ���Ͳ�õ�������������������Ͳ�ڵ�����ѹ������Ͳ�ڣ������±����еIJ�ͬʵ�飨ʵ��1��CO2�����Ϊ��״���£�����������ͬ��ͬѹ�²ⶨ����
��ͼ��ʾ�����ס�������װ�в�ͬ���ʵ���Ͳ�õ�������������������Ͳ�ڵ�����ѹ������Ͳ�ڣ������±����еIJ�ͬʵ�飨ʵ��1��CO2�����Ϊ��״���£�����������ͬ��ͬѹ�²ⶨ���� | ʵ����� | ����Ͳ������ | ����Ͳ������ | ����Ͳ������ |
| 1 | 10mL 0.1mol/LNaOH��Һ | 22.4mLCO2 | ���������� |
| 2 | 20mL H2S | 10mL SO2 | |
| 3 | 30mL NO2 | 10mL H2O��l�� | ʣ����ɫ���壬�����Զ�����ѹ�� |
| 4 | 15mL Cl2 | 40mL NH3 |


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
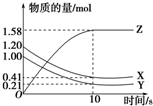 һ���¶��£���2L���ܱ������У�X��Y��Z������������ʵ�����ʱ��仯����������ͼ��ʾ������������ȷ���ǣ�������
һ���¶��£���2L���ܱ������У�X��Y��Z������������ʵ�����ʱ��仯����������ͼ��ʾ������������ȷ���ǣ�������| A����Ӧ��ʼ��10s����Z��ʾ�ķ�Ӧ����Ϊ0.158mol/��L?s�� |
| B����Ӧ��ʼ��10s��X�����ʵ���Ũ�ȼ�����0.79mol/L |
| C����ƽ��ʱY�����ʵ�������Ϊ��9.5% |
| D����Ӧ�Ļ�ѧ����ʽΪ��X��g��+Y��g��?Z��g�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A�����ʱ�������õ��������������õ������� |
| B�������������л���ɫ��������� |
| C����������������Һ�е����̪��Һ����Һ����ɫ |
| D�����һ��ʱ������Һȫ��ת�Ƶ��ձ��У���ֽ������Һ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��c��H+����c��F-�� |
| B��c��H+����c��HF�� |
| C��c��OH-����c��HF�� |
| D��c��HF����c��F-�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A | B | C | D | |
| װ�� | 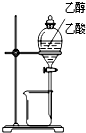 | 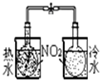 | 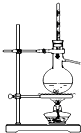 |  |
| ʵ�� | �����Ҵ������� | ֤���¶ȶԻ�ѧƽ���Ӱ�� | ����е����ϴ�Ļ���Һ������ | ��ȡ���ռ����� |
| A��A | B��B | C��C | D��D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
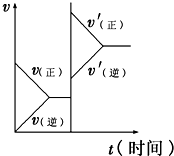 ���ڴﵽƽ��Ŀ��淴Ӧ��X+Y?W+Z������ѹǿ�������淴Ӧ���ʣ�v���ı仯��ͼ��ʾ��������֪X��Y��Z��W�ľۼ�״̬�����ǣ�������
���ڴﵽƽ��Ŀ��淴Ӧ��X+Y?W+Z������ѹǿ�������淴Ӧ���ʣ�v���ı仯��ͼ��ʾ��������֪X��Y��Z��W�ľۼ�״̬�����ǣ�������| A��X��Y��Z��W��Ϊ���� |
| B��Z��WΪ���壬X��Y��֮һΪ���� |
| C��X��Y��Z��Ϊ���壬WΪ������ |
| D��X��YΪ���壬Z��W��������һ��Ϊ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ���ʵ��� | CO2 | H2 | CH3OH��g�� | H2O |
| �� | a mol | a mol | 0mol | 0mol |
| �� | 2a mol | a mol | 0mol | 0mol |
| �� | 0mol | 0mol | a mol | a mol |
| �� | a mol | 0mol | a mol | a mol |
| A���� | B���� | C���� | D���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ���ܱ������м����Ũ�ȵ�CO��H2O��T��ʱ�������·�Ӧ��
���ܱ������м����Ũ�ȵ�CO��H2O��T��ʱ�������·�Ӧ���鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com