
| A. | ①③⑤ | B. | ①③⑥ | C. | ②③④ | D. | ①④⑥ |
分析 ①FeS2在高温下氧化可以生成二氧化硫,二氧化硫能够被双氧水氧化成硫酸;
②二氧化硫不与盐酸发生反应;
③铝与氢氧化钠溶液反应生成偏铝酸钠和氢气,偏铝酸钠加热蒸发可以获得偏铝酸钠;
④稀盐酸不与二氧化锰反应,无法用稀盐酸获得氯气;
⑤氢氧化铜浊液与葡萄糖加热反应生成的是氧化亚铜,不会得到氧化铜;
⑥根据侯氏制碱法原理进行判断.
解答 解:①煅烧FeS2可以得到SO2,二氧化硫具有还原性,能够被双氧水氧化成硫酸,该转化关系均可以一步实现,故①正确;
②二氧化硫难溶于水,二氧化硅不与盐酸反应,则SiO2$\stackrel{HCl(aq)}{→}$SiCl4不能一步实现,故②错误;
③金属Al能够与氢氧化钠溶液反应生成偏铝酸钠,蒸发偏铝酸钠溶液可以获得偏铝酸钠,所以转化关系Al$\stackrel{NaOH(ap)}{→}$NaAlO2(aq)$\stackrel{蒸发}{→}$NaAlO2(s)均能一步实现,故③正确;
④1mol•L-1HCl(aq)的盐酸为稀盐酸,稀盐酸不与二氧化锰反应,无法用稀盐酸与二氧化锰反应制取氯气,故④错误;
⑤Cu(OH)2$→_{△}^{葡萄糖}$生成的是Cu2O,直接加热氢氧化铜可获得CuO,故⑤错误;
⑥向饱和氯化钠溶液中通入氨气,然后通入二氧化碳可以获得碳酸氢钠固体,加热碳酸氢钠可以分解得到碳酸钠,所以转化关系饱和NaCl溶液$\stackrel{NH_{3}、CO_{2}}{→}$NaHCO3$\stackrel{△}{→}$Na2CO3均可以一步实现,故⑥正确;
故选B.
点评 本题考查了常见金属及其化合物性质,题目难度中等,明确常见元素及其化合物性质为解答关键,④为易错点,注意稀盐酸不与二氧化锰反应,试题有利于提高学生的分析能力及灵活应用能力.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 若R(OH)n为强碱,则W(OH)m也为强碱 | |
| B. | 若HnXOm为强酸,则Y是活泼非金属元素 | |
| C. | 若Y 的最低负化合价为一2,则Z的最高正化合价为+7 | |
| D. | 若X 的最高正化合价为十5,则五种元素一定都是非金属元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2mol气态H2与1mol气态氧气完全燃烧生成2mol液态水时放出571.6 kJ的热量 | |
| B. | 1mol气态H2与0.5mol气态氧气完全燃烧生成1mol液态水时吸收285.8kJ的热量 | |
| C. | 2个氢分子完全燃烧生成液态水时放出571.6 kJ的热量 | |
| D. | 上述热化学方程式可表示为H2(g)+O2(g)=H2O(1),H=-285.8 kJ•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
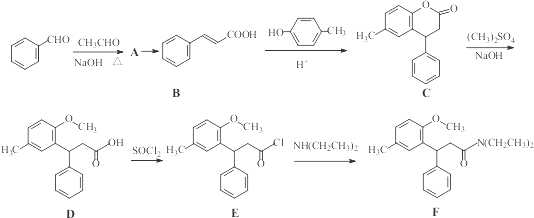
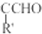
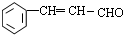 .
.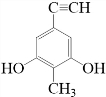 等.(任写一种)
等.(任写一种)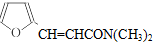 )是一种高效麻醉剂,写出以
)是一种高效麻醉剂,写出以 、CH3CHO、NH(CH3)2为原料制备呋喃丙胺的合成路线流程图(无机试剂自选).合成路线流程图示例如下:
、CH3CHO、NH(CH3)2为原料制备呋喃丙胺的合成路线流程图(无机试剂自选).合成路线流程图示例如下:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 离子结构示意图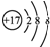 :可以表示35Cl-,也可以表示37Cl- :可以表示35Cl-,也可以表示37Cl- | |
| B. | 电子式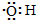 :可以表示羟基,也可以表示氢氧根离子 :可以表示羟基,也可以表示氢氧根离子 | |
| C. | 比例模型 :可以表示甲烷分子,也可以表示四氯化碳分子 :可以表示甲烷分子,也可以表示四氯化碳分子 | |
| D. | 聚丙烯的结构简式: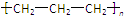 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
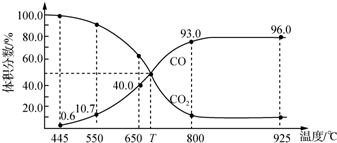
| A. | 550℃时,若充入惰性气体,v(正)、v(逆)均减小,平衡不移动 | |
| B. | 650℃时,反应达平衡后CO2的转化率为25.0% | |
| C. | T℃时,若充入等体积的CO2和CO,平衡向逆反应方向移动 | |
| D. | 925℃时,此反应的平衡常数K=2 304,保持温度不变,若缩小体积,K值将变小 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
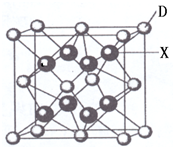 已知A、B、C、D、E都是周期表中前四周期的元素,它们的核电荷数A<B<C<D<E.其中A、B、C是同一周期的非金属元素.化合物DC 2的晶体为离子晶体,其阳离子与阴离子的个数比为1:1,D的二价阳离子比C的简单阴离子多一个电子层.AC 2为非极性分子.B、C的氢化物的沸点比它们同族相邻周期元素氢化物的沸点高.E原子序数为26.回答下列问题:(答题时,A、B、C、D、E用所对应的元素符号表示).
已知A、B、C、D、E都是周期表中前四周期的元素,它们的核电荷数A<B<C<D<E.其中A、B、C是同一周期的非金属元素.化合物DC 2的晶体为离子晶体,其阳离子与阴离子的个数比为1:1,D的二价阳离子比C的简单阴离子多一个电子层.AC 2为非极性分子.B、C的氢化物的沸点比它们同族相邻周期元素氢化物的沸点高.E原子序数为26.回答下列问题:(答题时,A、B、C、D、E用所对应的元素符号表示).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 光导纤维应避免在强碱环境中使用 | |
| B. | 船体镀锌或镀锡均可保护船体,镀层破损后将立即失去保护作用 | |
| C. | 利用碳酸酯聚合材料生产一次性饭盒,可以减少对环境产生的白色污染 | |
| D. | 油脂皂化生成的高级脂肪酸钠是肥皂的有效成分 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 滴加硫酸酸化的FeSO4溶液,平衡不移动 | |
| B. | 溶液颜色保持不变时,该反应达到平衡状态 | |
| C. | 滴加6 mol/L NaOH溶液,溶液颜色变深 | |
| D. | 平衡常数表达式为K=$\frac{2c(Cr{{O}_{4}}^{2-})•2c({H}^{+})}{c(C{r}_{2}{{O}_{7}}^{2-})•c({H}_{2}O)}$ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com