

���� Aװ����C��Ũ���ᷢ��������ԭ��Ӧ����NO2����Ӧ����ʽΪC+4HNO3��Ũ��=CO2��+4NO2��+2H2O��NO2ͨ��B�к�ˮ������Ӧ3NO2+H2O=2HNO3+NO��Cu��ϡ���ᷢ����Ӧ3Cu+8HNO3=3CuNO3+2NO��+4H2O��C�з�����Ӧ 2NO+Na2O2=2NaNO2��ʣ���NO�����Ը��������Һ�����������ᣬ
��1��a�Ƿ�Һ©����NO�ж�����ֱ���ſգ�
��2��C��HNO3��Ũ��������Ӧ����CO2��NO2��H2O��NO��Na2O2������Ӧ����NaNO2��
��3��a��A�����ɶ�����̼��������̼�������Ʒ�Ӧ����̼���ƣ�̼������ҺҲ�ʼ��ԣ�
b�����������ܺ�ϡ���ᷴӦ������ɫ����NO��NO���ȶ��ױ������������ɺ���ɫ�������������
��4���ٴ�Bװ���г����������к���NO��������̼��ˮ�������⼸�����ʶ��ܺ������Ʒ�Ӧ��ҪʹC��ֻ��NO�������Ʒ�Ӧ����BCװ�ü��Eװ��Ӧ��������ˮ�����Ͷ�����̼��
��Ҫ�ų�����������ֹ��Ӧ��Ӧ����ͨ��һ��ʱ��ĵ�����
��� �⣺��1��a�����Ƿ�Һ©����NO�ж�����ֱ���ſգ�NO�����Ը��������Һ��Ӧ������������Ӻ������ӣ��Ӷ���ȥNO��
�ʴ�Ϊ����Һ©������ȥδ��Ӧ��NO����ֹ��Ⱦ������
��2��C��HNO3��Ũ��������Ӧ����CO2��NO2��H2O����Ӧ����ʽΪC+4HNO3��Ũ��$\frac{\underline{\;\;��\;\;}}{\;}$CO2��+4NO2��+2H2O��NO��Na2O2������Ӧ����NaNO2����Ӧ����ʽΪ 2NO+Na2O2=2NaNO2��
�ʴ�Ϊ��C+4HNO3��Ũ��$\frac{\underline{\;\;��\;\;}}{\;}$CO2��+4NO2��+2H2O��2NO+Na2O2=2NaNO2��
��3��a��A�����ɶ�����̼��������̼�������Ʒ�Ӧ����̼���ƣ�̼������ҺҲ�ʼ��ԣ�B�г����������л�����ˮ�����ܺ�C�еĹ������Ʒ�Ӧ����NaOH���ʼ��ԣ����Բ��ܸ�����ˮ��Һ�жϺ����������ƣ���a����
b�����������ܺ�ϡ���ᷴӦ������ɫ����NO��NO���ȶ��ױ������������ɺ���ɫ���������������ʵ������˵�������������ƣ���b��ȷ��
��ѡ��b��
��4���ٴ�Bװ���г����������к���NO��������̼��ˮ�������⼸�����ʶ��ܺ������Ʒ�Ӧ��ҪʹC��ֻ��NO�������Ʒ�Ӧ����BCװ�ü��Eװ��Ӧ��������ˮ�����Ͷ�����̼��ʹ�õ�ҩƷ�Ǽ�ʯ�ң�
�ʴ�Ϊ����ʯ�ң�
��Ҫ�ų�������ֹ������Ӧ��Ӧ����ͨ��һ��ʱ��ĵ������ʴ�Ϊ�����ɼУ�ͨ��N2һ��ʱ�䣮
���� ���⿼�������Ʊ���Ϊ��Ƶ���㣬�漰������ԭ��Ӧ�����ʼ��顢ʵ�������ʵ�����ۼ�����ʽ�����֪ʶ�㣬��ȷ��ѧ��Ӧԭ����ʵ����������������������ʲ������ǽⱾ��ؼ���ע��ʵ��������Է����жϣ���Ŀ�Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
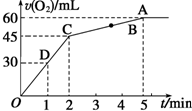 ����0.1mol MnO2��ĩ��50mL����������Һ����=1.1g•mL-1���У��ڱ�״���·ų�����������ʱ��Ĺ�ϵ��ͼ��ʾ��
����0.1mol MnO2��ĩ��50mL����������Һ����=1.1g•mL-1���У��ڱ�״���·ų�����������ʱ��Ĺ�ϵ��ͼ��ʾ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Ư���ڿ����в��ȶ���������Ư��ֽ�� | |
| B�� | Ư���е�CaCl2������е�CO2��Ӧ������CaCO3��Ư���ڿ����о��ñ��� | |
| C�� | NH3��ʹ��̪��Һ��죬���NH3�����������Ȫʵ�� | |
| D�� | ��ĥ��ʯ��ָ���벻�漰��ѧ��Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| �¶� | 250�� | 300�� | 350�� |
| K | 2.041 | 0.270 | 0.012 |
| CO | H2 | CH3OH |
| 0.5mol•L-1 | 2mol•L-1 | 6mol•L-1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
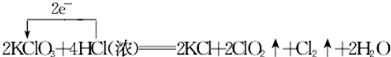 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com