
关于如图所示的原电池,下列说法正确的是()
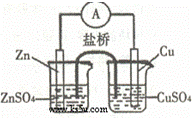
A. 电子从锌电极通过检流计流向铜电极
B. 盐桥中的阴离子向硫酸铜溶液中迁移
C. 锌电极发生还原反应,铜电极发生氧化反应
D. 铜电极上发生的电极反应是2H++2e﹣=H2↑
考点: 原电池和电解池的工作原理.
专题: 电化学专题.
分析: 该原电池中,较活泼的金属作负极,负极上失电子发生氧化反应;较不活泼的金属作正极,正极上得电子发生还原反应;电子从负极沿导线流向正极,盐桥中的阴离子向硫酸锌溶液中迁移,阳离子向硫酸铜溶液中迁移.
解答: 解:A、该原电池中较活泼的金属锌作负极,较不活泼的金属铜作正极,电子从锌电极通过检流计流向铜电极,故A正确.
B、原电池放电时,盐桥中的阴离子向硫酸锌溶液中迁移,阳离子向硫酸铜溶液中迁移,故B错误.
C、原电池放电时,锌作负极,锌失电子发生氧化反应,铜作正极,铜离子得电子发生还原反应在铜极上析出,故C错误.
D、原电池放电时,铜作正极,铜离子得电子发生还原反应在铜极上析出,电极反应式为Cu2++2e﹣=Cu,故D错误.
故选A.
点评: 本题考查了原电池原理,难度不大,明确原电池放电时盐桥中阴阳离子的移动方向.


 心算口算巧算一课一练系列答案
心算口算巧算一课一练系列答案科目:高中化学 来源: 题型:
酒精和醋酸是生活里的常用品,下列方法不能将二者鉴别开的是( )
|
| A. | 闻气味 |
|
| B. | 分别用来浸泡水壶中的水垢看是否溶解 |
|
| C. | 分别滴加NaOH溶液 |
|
| D. | 分别滴加石蕊试液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
能说明醋酸是弱电解质的事实是()
A. 醋酸水溶液能使湿润的蓝色石蕊试纸变红
B. 醋酸和碳酸钠溶液反应放出二氧化碳
C. c(H+)相同的醋酸和盐酸相比较,醋酸溶液的浓度大
D. 浓度和体积均相同的醋酸和盐酸可中和等物质的量的NaOH
查看答案和解析>>
科目:高中化学 来源: 题型:
在0.1mol•L﹣1 CH3COOH溶液中存在如下电离平衡:CH3COOH⇌CH3COO﹣+H+,对于该平衡,下列叙述正确的是()
A. 加入水时,平衡向逆反应方向移动
B. 加入少量NaOH固体,平衡向正反应方向移动
C. 加入少量0.1mol•L﹣1 HCl溶液,溶液中c(H+)减小
D. 加入少量CH3COONa固体,平衡向正反应方向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
如图所示的装置,C、D、E、F均为惰性电极.将电源接通后,向乙中滴入酚酞溶液,在F极附近显红色.试回答下列问题:(1)电极A是正极填“正极”或“负极”)
(2)甲装置中C极的电极反应式为.
(3)若用惰性电极电解饱和NaCl溶液一段时间,当阳极产生56 mL(标准状况下)气体,电解后溶液体积为500 mL时,所得溶液在25℃时的pH=.
(4)欲用丙装置给铜镀银,G应该是银(填“铜”或“银”),电镀液的主要成分是(填化学式).

查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验所对应的离子方程式正确的是()
A. 向NaAlO2溶液中通入少量CO2:AlO2﹣+CO2+2H2O═Al(OH)3↓+HCO3﹣
B. 向沸水中滴加饱和的氯化铁溶液:Fe3++3H2O═Fe(OH)3↓+3H+
C. 在碳酸氢钡溶液中加入过量的氢氧化钠溶液:Ba2++2HCO3﹣+2OH﹣═BaCO3↓+CO32﹣+2H2O
D. 向FeCl2溶液中加入少量K3[Fe(CN)6]溶液:4Fe2++2[Fe(CN)6]4﹣═Fe4[Fe(CN)6]2↓
查看答案和解析>>
科目:高中化学 来源: 题型:
在已经处于化学平衡状态的体系中,如果下列量发生变化,其中一定能表明化学平衡移动的是 ( )
A.反应混合物的浓度 B. 反应体系的压强
C.正、逆反应的速率 D. 反应物的转化率
查看答案和解析>>
科目:高中化学 来源: 题型:
将30mL0.5mol/LNaOH溶液加水稀释到500mL,稀释后溶液的浓度为()
A. 0.1mol/L B. 0.3mol/L C. 0.05mol/L D. 0.03mol/L
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com