
【题目】下列属于电解质的是( )
A.硫酸钠B.蔗糖C.盐酸D.二氧化硫
 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案科目:高中化学 来源: 题型:
【题目】二氧化硫、氮气、二氧化碳组成的混合气体在同温、同压下与笑气(N 2O)的密度相同,则该 混合气体中二氧化硫、氮气、二氧化碳的质量比为( )
A. 4:5:6 B. 22:1:14
C. 64:35:13 D. 29:8:13
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苯氧乙醇是护肤产品中常用的一种有机物,下图是利用烃M和苯酚为主要原料制备苯氧乙醇的合成路线,请回答相关问题。
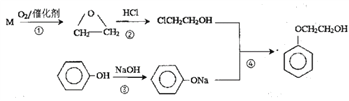
(1)反应①中M与氧气的物质的量之比为2:1且原子利用率为100%,则M的结构简式是_______________,反应①的反应类型是___________________。
(2)ClCH2CH2OH的名称是_____________________。
(3)苯氧乙醇中含有的官能团是___________________,分子式是___________________。
(4)苯酚除了与氢氧化钠反应外也可以与碳酸钠反应生成苯酚钠,该反应的化学方程式是_____________
(5)苯氧乙醇的同分异构体中符合下列要求的有__________种(不考虑一个碳原子上连两个羟基的情况)。
a.属于芳香化合物且苯环上有奇数个取代基
b.能与钠反应生成氢气且只含有一种官能团
其中核磁共振氢谱中峰的数目最少的结构简式为_________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子中,能在溶液中大量共存的一组是( )
A.Al3+、NH4+、OH-B.Na+、Ba2+、SO42-
C.K+、Fe3+、I-D.K+、NO3-、HCO3-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硼普遍存在于蔬果中,是维持骨的健康和钙、磷、镁正常代谢所需要的微量元素之一。回答下列问题:
(1)硼原子核外电子占据最高能层的符号是__________,占据最高能级的电子云轮廓图形状为___________。价层电子的轨道表达式(电子排布图)为____________。
(2)硼原子的第二电高能(I2)和第三电离能(I3)的大小关系为:I2______I3(填“>”或“<”),原因是____________。
(3)BF3可用于制造火箭的高能燃料。其分子构型为___________,已知BF3分子中F原子和B原子采用同种杂化方式为____________,BF3分子还中存在大π键,可用符号![]() 表示(其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数,如苯分子中的大π键可表示为
表示(其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数,如苯分子中的大π键可表示为![]() ),则分子中的大π键应表示为____________。
),则分子中的大π键应表示为____________。
(4)硼酸(H3BO3)晶体为层状结构。其中一层的结构片段如图(a)所示,将这些H3BO3分子聚集在一起的作用为____________。
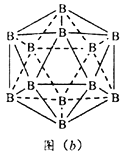
(5)晶体拥有多种变体,但其基本结构单元都是由硼原子组成的正二十面体,如图(b),每个顶点为个硼原子,构成的三角形均为等边三角形,若该结构单元中有10个原子为10B(其余为11B),那么该结构单元有_________种不同类型。
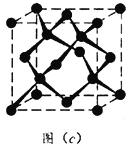
(6)立方氮化硼(BN)晶体与金刚石晶体互为等电子体,图(c)为金刚石晶体的晶胞,立方氮化硼晶体可以取出多种晶胞。其中一种晶胞中N全部位于晶胞体内,则B处于____________位置。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究CO2的利用对促进低碳社会的构建具有重要意义。
(1)将CO2与焦炭作用生成CO,CO可用于炼铁等。
①已知: ![]()
![]()
则CO还原Fe2O3(s)的热化学方程式为________________________________。
(2)常温下,用氨水吸收CO2可得到NH4HCO3溶液。已知常温下:NH3·H2O的电离平衡常数Kb=2×10-5,H2CO3的电离平衡常数K1=4×10-7,K2=4×10-11。在NH4HCO3溶液中,c(NH4+)______c(HCO3-)(填“>”“<”或“=”),计算反应NH4+ + HCO3- + H2O NH3·H2O + H2CO3的平衡常数K=______________,物料守恒表达式为__________________________。
(3)以CO2为原料还可以合成多种物质。
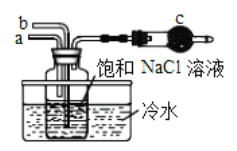
①如图是模拟“侯氏制碱法”制取NaHCO3的部分装置。操作中先在_______处向饱和NaCl溶液中通入_________气体(填NH3或CO2),然后再在通入另一种气体。请写出反应的化学方程式_______________________。
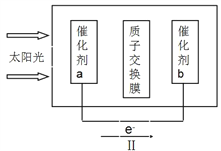
②人工光合作用能够借助太阳能用CO2和水制备化学原料,如图是通过人工光合作用制备HCOOH的原理示意图,请写出催化剂b处的电极反应式:____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)标准状况下,5.6 L A气体的质量是15 g ,则A的相对原子质量为___。
(2)一定量的液态化合物XY2,与一定量O2在一密闭容器中恰好完全反应:XY2(液)+3O2(气)=XO2(气)+2YO2(气),冷却至标准状况,测得容器内气体的体积为6.72L,密度为2.5g/L。则:化合物XY2的摩尔质量为________。
(3)质量之比为16:7:6的三种气体SO2、CO、NO,分子数之比为___________,氧原子数之比为__________,相同条件下的体积之比为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学生欲用0.100 0 mol·L-1的盐酸来滴定未知浓度的氢氧化钠溶液时,选择酚酞作指示剂。请填写下列空白:
(1)用0.100 0 mol·L-1的盐酸溶液滴定待测的氢氧化钠溶液时,左手把握酸式滴定管的活塞,右手摇动锥形瓶,眼睛注视____________。直到因加入一滴盐酸后,溶液由红色变为无色,且____________为止。
(2)若滴定开始和结束时,酸式滴定管中的液面如图所示:则起始读数为____________mL,终点读数为____________mL。

(3)某学生根据三次实验分别记录有关数据如下:
滴定次数 | 氢氧化钠溶液/mL | 0.100 0 mol·L-1 盐酸的体积(mL) | ||
滴定前 | 滴定后 | 消耗 | ||
第一次 | 25.00 | 0.00 | 26.11 | 26.11 |
第二次 | 25.00 | 1.56 | 30.30 | 28.74 |
第三次 | 25.00 | 0.22 | 26.31 | 26.09 |
请选用其中合理的数据列式计算该氢氧化钠溶液的物质的量浓度:c(NaOH)=______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com