
| A. | 硫酸的摩尔质量是98 g•mol-1 | |
| B. | 2 mol NO和1 mo1 NO2所含的氧元素质量相同 | |
| C. | 等质量的02和03所含氧原子数相等 | |
| D. | 等物质的量的CO和CO2所含氧原子数相等 |
分析 A.硫酸的相对分子质量为98,据此可判断硫酸的摩尔质量;
B.2 mol NO和1 mo1 NO2都含有2mol氧原子;
C.氧气和臭氧分子中都只含有氧元素,则质量相等时二者含有的氧原子数相等;
D.CO和二氧化碳分子中含有的氧原子数不相等.
解答 解:A.硫酸的相对分子质量为98,则其摩尔质量是98 g•mol-1,故A正确;
B.2 mol NO和1 mo1NO2所含的氧原子都是2mol,所以氧元素的质量相同,故B正确;
C.氧气和臭氧都只含有氧原子,所以等质量时二者含有的氧原子的数目相等,故C正确;
D.一氧化碳中氧原子的数目为二氧化碳中的一半,故D错误;
故选D.
点评 本题考查了物质的量的计算,题目难度不大,明确物质的量与摩尔质量、阿伏伽德罗常数等之间的关系即可解答,试题有利于培养学生的化学计算能力.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:多选题
| A. | 稀硫酸滴在铜片上:Cu+2H+═Cu2++H2 | |
| B. | 氧化铜与硫酸反应:O2-+2 H+═H2O | |
| C. | 硫酸钠和氯化钡两种溶液混合:Ba2++SO42-═BaSO4↓ | |
| D. | 盐酸与石灰石反应:CaCO3+2H+═Ca2++H2O+CO2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 元素代号 | A | B | C | D | E |
| 原子半径/nm | 0.16 | 0.143 | 0.102 | 0.099 | 0.074 |
| 主要化合价 | +2 | +3 | +6、-2 | -1 | -2 |
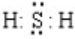 .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 油脂分子中都含有碳碳双键 | B. | 葡萄糖分子中含有羟基和醛基 | ||
| C. | 水分子中含有羟基 | D. | 乙酸乙酯分子中含有羧基 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 (1)20世纪30年代,Eyring和Pzer在碰撞理论的基础上提出化学反应的过渡态理论:化学反应并不是通过简单的碰撞就能完成的,而是在反应物到生成物的过程中经过一个高能量的过渡态.如图是NO2和CO反应生成CO2和NO过程中的能量变化示意图,说明这个反应是放热(填“吸热”或“放热”)反应,NO2和CO的总能量大于(填“大于”、“小于”或“等于”)CO2和NO的总能量.
(1)20世纪30年代,Eyring和Pzer在碰撞理论的基础上提出化学反应的过渡态理论:化学反应并不是通过简单的碰撞就能完成的,而是在反应物到生成物的过程中经过一个高能量的过渡态.如图是NO2和CO反应生成CO2和NO过程中的能量变化示意图,说明这个反应是放热(填“吸热”或“放热”)反应,NO2和CO的总能量大于(填“大于”、“小于”或“等于”)CO2和NO的总能量.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
 已知:A、B、C、D、E、F六种元素核电荷数依次增大,属于周期表中前四周期的元素.其中A原子核外有三个未成对电子;化合物B2E的晶体为离子晶体,E原子核外的M层中只有两对成对电子;C元素是地壳中含量最高的金属元素;D单质的熔点在同周期元素形成的单质中是最高的;F原子核外最外层电子数与B相同,其余各层均充满.请根据以上信息,回答下列问题:
已知:A、B、C、D、E、F六种元素核电荷数依次增大,属于周期表中前四周期的元素.其中A原子核外有三个未成对电子;化合物B2E的晶体为离子晶体,E原子核外的M层中只有两对成对电子;C元素是地壳中含量最高的金属元素;D单质的熔点在同周期元素形成的单质中是最高的;F原子核外最外层电子数与B相同,其余各层均充满.请根据以上信息,回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加水稀释溶液,[OH-]减小 | |
| B. | 加入NaOH固体,$\frac{[S{O}_{3}^{2-}]}{[{H}_{2}S{O}_{3}]}$增大 | |
| C. | 升高温度,②的平衡常数K增大 | |
| D. | 加入硝酸,[H2SO3]减小 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com