
| 甲 | 乙 | |
| 丙 | 丁 | 戊 |
| A. | 原子半径:甲<乙<丙 | B. | 金属性:甲<丙 | ||
| C. | 氢氧化物碱性:丙>丁>戊 | D. | 最外层电子数:甲<乙 |
分析 由短周期金属元素甲~戊在周期表中的相对位置可知,甲为Li,乙为Be,丙为Na,丁为Mg,戊为Al,然后结合元素周期律来解答.
解答 解:由短周期金属元素甲~戊在周期表中的相对位置可知,甲为Li,乙为Be,丙为Na,丁为Mg,戊为Al,
A.电子层越多,原子半径越大,同周期从左向右原子半径减小,则原子半径:乙<甲<丙,故A错误;
B.同主族从上到下金属性增强,则金属性:甲<丙,故B正确;
C.同周期从左向右金属性减弱,则对应碱的碱性减弱,可知氢氧化物碱性:丙>丁>戊,故C正确;
D.同周期从左向右最外层电子数增大,则最外层电子数:甲<乙,故D正确;
故选A.
点评 本题考查位置、结构及应用,为高频考点,把握元素的位置、元素周期律为解答的关键,注意规律性知识的应用,侧重分析与应用能力的考查,题目难度不大.


科目:高中化学 来源: 题型:解答题
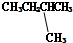 D、H2 和D2
D、H2 和D2查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 绿色食品是指不含任何化学物质的食品 | |
| B. | 硅是制造太阳能电池的常用材料 | |
| C. | NaOH溶液可以盛装在带橡皮塞的试剂瓶中 | |
| D. | 光导纤维是以二氧化硅为主要原料制成的 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C3H8与C2H6互为同系物 | |
| B. | 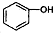 与 与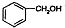 互为同系物 互为同系物 | |
| C. | 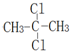 和 和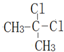 是同一种物质 是同一种物质 | |
| D. | 化学式为C5H10的有机物不一定能使溴的四氯化碳溶液褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NH3、NO2 | B. | NaCl、KF | C. | NaOH、Ca(OH)2 | D. | MgO、H2O2 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 物质发生化学反应时都伴随着能量变化,伴随着能量变化的物质变化一定是化学变化 | |
| B. | 需要加热的化学反应一定是吸热反应,不需要加热就能进行的反应一定是放热反应 | |
| C. | 化学变化中的能量变化主要是由化学键变化引起的 | |
| D. | 因为石墨变成金刚石吸热,所以金刚石比石墨稳定 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. |  | B. | 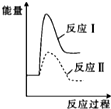 | C. | 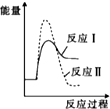 | D. | 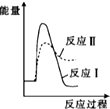 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
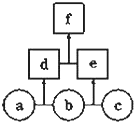 如图所示,a、b、c均为非金属单质,d、e均为含有10个电子的共价化合物,且分子中所含原子个数:d>e,f为离子化合物.则下列说法错误的是( )
如图所示,a、b、c均为非金属单质,d、e均为含有10个电子的共价化合物,且分子中所含原子个数:d>e,f为离子化合物.则下列说法错误的是( )| A. | d和e分子中所有原子都不满足8电子结构 | |
| B. | 单质c的氧化性强于单质a | |
| C. | 相同状况下,单质c、a、b的沸点逐渐减小 | |
| D. | f可电离生成两种含10个电子的离子 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com