
| A、FeCl3溶液 |
| B、NaHCO3溶液 |
| C、Na2SO3溶液 |
| D、CH3COONa溶液 |


科目:高中化学 来源: 题型:
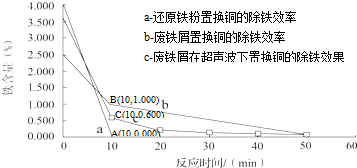
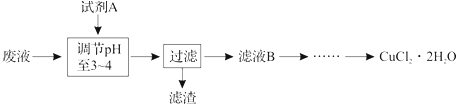
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Cu(OH)2 |
| 开始沉淀 | 2.3 | 7.5 | 4.7 |
| 完全沉淀 | 4.1 | 9.7 | 6.7 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 温度/℃ | 200 | 300 | 400 | 500 | 600 |
| 氨含量/% | 89.9 | 71.0 | 47.0 | 26.4 | 13.8 |
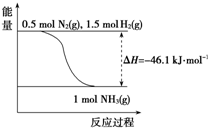
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、25℃时1g镁投入100ml 0.5mol/L盐酸溶液中 |
| B、25℃时1g镁投入200ml 0.5mol/L盐酸溶液中 |
| C、25℃时1g镁投入50ml 1mol/L盐酸溶液中 |
| D、50℃时1g镁投入10ml 1mol/L盐酸溶液中 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、原子半径:Cl>Mg>Na |
| B、酸性:H2SiO3>H2CO3>HNO3 |
| C、稳定性:HF<NH3<CH4 |
| D、碱性:LiOH<NaOH<KOH |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用量筒量取所需的盐酸时俯视刻度线 |
| B、定容时,仰视刻度线 |
| C、用量筒量取所需浓盐酸注入盛有适量蒸馏水的烧杯后,再分别用少量蒸馏水洗涤玻璃棒、量筒2-3次,洗涤液注入25 0 mL容量瓶中 |
| D、定容后倒转容量瓶几次,发现凹液面最低点低于刻度线,再补几滴水到刻度线 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com