
| A、2 mol C |
| B、1 mol B和1 mol C |
| C、2 mol A、1 mol B |
| D、3 mol A、0.5 mol B |
| 4 |
| 3 |
| 2 |
| 3 |
| 2 |
| 3 |
| 4 |
| 3 |


 口算题天天练系列答案
口算题天天练系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
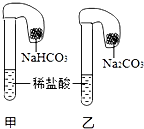 按如图装置进行实验,气球中装有等质量的Na2CO3与NaHCO3,试管中装有等浓度的足量的稀盐酸,把两种药品同时倒入试管中,下列说法正确的是( )
按如图装置进行实验,气球中装有等质量的Na2CO3与NaHCO3,试管中装有等浓度的足量的稀盐酸,把两种药品同时倒入试管中,下列说法正确的是( )| A、甲中气球膨胀得大 |
| B、两气球膨胀一样大 |
| C、甲中消耗的盐酸多 |
| D、乙中气球膨胀得快 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 测定时刻/s | t1 | t2 | t3 | t4 |
| C(A)/mol?L-1 | 6 | 3 | 2 | 2 |
| C(B)/mol?L-1 | 5 | 3.5 | 3 | 3 |
| C(C)/mol?L-1 | 1 | 2.5 | 3 | 3 |
| A、在容器中发生的反应为2A(g)+B(g)?2C(g) |
| B、该温度下,此反应的平衡常数为0.25 |
| C、A的转化率比B转化率的低 |
| D、在t3时刻反应已经停止 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| PCl3(g) | Cl2(g) | PCl5(g) | |
| 初始浓度(mol/L) | 2.0 | 1.0 | 0 |
| 平衡浓度(mol/L) | c1 | c2 | 0.4 |
| A、若升高温度,反应的平衡常数减小,则正反应为吸热 |
| B、反应5min内,v(PCl3)=0.08 mol?L-1?min-1 |
| C、当容器中Cl2为1.2mol时,可逆反应达到平衡状态 |
| D、平衡后移走2.0mol PCl3和1.0mol Cl2,在相同条件下再达平衡时,c(PCl5)<0.2 mol?L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①②③⑥ | B、①③④⑥ |
| C、③④⑤⑥ | D、全部 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、8000ab/V |
| B、8000Vb/a |
| C、16000Vb/a |
| D、16000ab/V |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、加热能杀死流感病毒是因为病毒的蛋白质受热发生变性 |
| B、乙醇和汽油都是可再生能源,应大力推广使用“乙醇汽油” |
| C、石油的分馏和煤的干馏都是物理变化 |
| D、糖类、油脂、蛋白质一定都能发生水解反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 )的合成路线如下:
)的合成路线如下: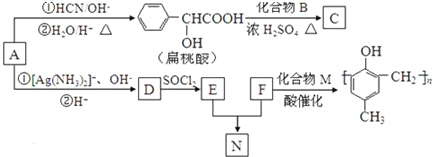
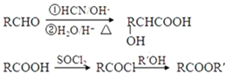 ,F分子式为C7H8O,
,F分子式为C7H8O,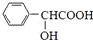 )有多种同分异构体,其中满足下述条件的同分异构体有
)有多种同分异构体,其中满足下述条件的同分异构体有查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com