
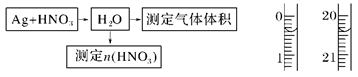
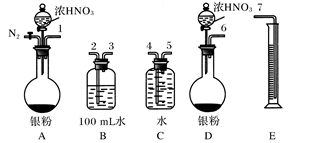
 N2O4,部分NO2转化为N2O4,致使测得的实际体积小于理论值
N2O4,部分NO2转化为N2O4,致使测得的实际体积小于理论值
 =89.6ml,但小于实验测得NO的体积为112.0 mL,故一定有NO生成
=89.6ml,但小于实验测得NO的体积为112.0 mL,故一定有NO生成

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:不详 题型:单选题
| A.1:1 | B.2:3 | C.3:2 | D.4:3 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.NH3 | B.CO2 | C.H2O(气) | D.O2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
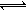 3HF △H>0, H2F2
3HF △H>0, H2F2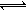 2HF △H>0。
2HF △H>0。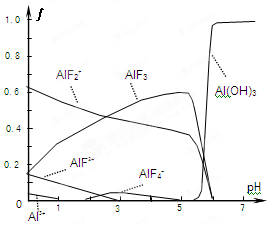
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
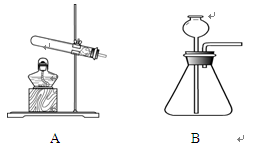
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
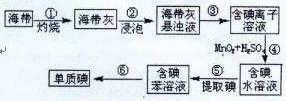
| A.酸性 | B.碱性 | C.氧化性 | D.还原性 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 璃窗,中间带有一根玻璃短柄。用此仪器进行有关实验时,具有装置简单、操作方便、现象明显、可反复使用等优点。用此仪器不能反复进行的实验是
璃窗,中间带有一根玻璃短柄。用此仪器进行有关实验时,具有装置简单、操作方便、现象明显、可反复使用等优点。用此仪器不能反复进行的实验是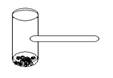
| A.NH4Cl受热分解的实验 |
| B.无水CuSO4与胆矾的互变实验 |
| C.白磷和红磷(已经抽出O2)在一定温度下相互转变的实验 |
| D.KMnO4受热分解的实验 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com