
| A、体积相等、质量不等的CO和N2 |
| B、等温等体积的O2和N2 |
| C、等体积等密度的CO和N2 |
| D、等压等体积的O2和N2 |
| m |
| M |
| m |
| M |
| V |
| Vm |
| m |
| M |
| V |
| Vm |


 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案科目:高中化学 来源: 题型:

| A、该反应符合绿色化学的原则 |
| B、聚碳酸酯质容器可长期盛放氢氧化钠溶液 |
C、环氧丙烷与环氧乙烷( )互为同系物 )互为同系物 |
| D、用聚碳酸酯代替聚乙烯、聚氯乙烯,可防止白色污染 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、甲、乙、丙形成的化合物既有离子键又有共价键 |
| B、乙、丙、丁形成的氢化物常温下均为气体 |
| C、原子序数由小到大顺序为:甲<乙<丙<丁 |
| D、原子半径大小顺序为:丁>甲>乙>丙 |
查看答案和解析>>
科目:高中化学 来源: 题型:
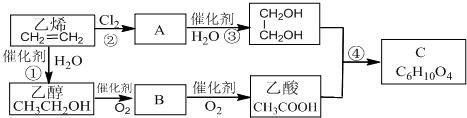
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、分子式为C16H18O9 |
| B、0.1mol绿原酸最多与0.8mol NaOH反应 |
| C、能发生取代反应和消去反应 |
| D、能与Na2CO3反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、金属X能与NaOH溶液反应放出H2,但金属Y不能,则Y的金属性一定比X弱 |
| B、在合成氨反应达到平衡时,只增加N2的物质的量,达新平衡后N2的百分含量增大 |
| C、在铁件上镀铜时,铁和电源负极相连,铜和正极相连,电解质溶液是CuSO4溶液 |
| D、Cl2和SO2等体积充分混合后,通入品红溶液,溶液颜色没有明显变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、H+、NO3-、Fe2+、Na+ |
| B、K+、Ba2+、OH-、SO42- |
| C、Fe2+、NO3-、I-、K+ |
| D、Cu2+、NH4+、Cl-、OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:
 反应aA(g)+bB(g)?cC(g)(△H<0)在等容条件下进行.改变其它反应条件,在I、Ⅱ、Ⅲ阶段体系中各物质浓度随时间变化的曲线如图所示,下列说法不正确的是( )
反应aA(g)+bB(g)?cC(g)(△H<0)在等容条件下进行.改变其它反应条件,在I、Ⅱ、Ⅲ阶段体系中各物质浓度随时间变化的曲线如图所示,下列说法不正确的是( )| A、反应的化学方程式中,a:b:c=1:3:2 |
| B、A的平均反应速率vⅠ(A)、vⅡ(A)、vⅢ(A),最大的是vⅠ(A) |
| C、第Ⅱ阶段反应温度小于第Ⅲ阶段反应温度 |
| D、由第一次平衡到第二次平衡,采取的措施是从反应体系中移走C |
查看答案和解析>>
科目:高中化学 来源: 题型:
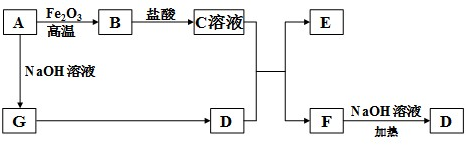
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com