
将cmolHCl与dmol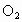 混合加到有催化剂的容器中,发生反应:
混合加到有催化剂的容器中,发生反应: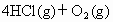
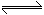
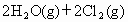 ,当有emol
,当有emol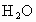 生成时达到平衡.求此时
生成时达到平衡.求此时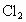 的质量分数和体积分数.
的质量分数和体积分数.
 英才点津系列答案
英才点津系列答案 红果子三级测试卷系列答案
红果子三级测试卷系列答案科目:高中化学 来源: 题型:阅读理解
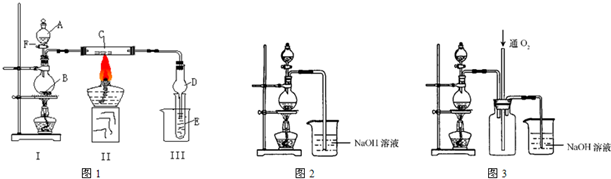
| ||
| ||
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
+ 4 |
+ 4 |
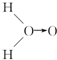 (式中O→O表示配位键,在化学反应中O→O键遇到还原剂时易断裂)
(式中O→O表示配位键,在化学反应中O→O键遇到还原剂时易断裂)

查看答案和解析>>
科目:高中化学 来源: 题型:
 Ⅰ.纯碱、烧碱等是重要的化工原料.
Ⅰ.纯碱、烧碱等是重要的化工原料.| 实验操作 | 实验现象 | 结论 |
| ①取少量白色固体于试管中,加水溶解,再加足量BaCl2溶液 | ||
| ②过滤,取2mL滤液于试管中, |
原白色固体中有OH-存在 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| KOH | O3 | A | KOH?H2O | 气体密度 |
| 16.8g | 0.3mol | a g | b g | >1.429g/L |
| 16.8g | 0.2mol | a g | b g | 1.429g/L |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com