
A、某溶液
| ||
B、某溶液
| ||
C、某溶液
| ||
D、某溶液
|


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、一定小于92.0 kJ |
| B、一定大于92.0 kJ |
| C、一定等于92.0 kJ |
| D、无法确定 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| >13.2℃ |
| <13.2℃ |
| A、△H1>△H2 |
| B、灰锡转化为白锡的反应是吸热反应 |
| C、锡制器皿应置于低于13.2℃的环境中,否则会自行毁坏 |
| D、锡的两种同素异形体在常温下可以相互转化,是可逆反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 |
| 2 |
| A、CO的燃烧热为283 kJ |
B、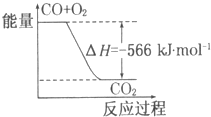 如图可表示由CO生成CO2的反应过程和能量关系 |
| C、2Na2O2(s)+2CO2(s)=2Na2CO3(s)+O2(g)△H=-452 kJ/mol |
| D、CO(g)与Na2O2(s)反应放出509 kJ热量时,电子转移数为2x6.02×l023 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 现有Al2(SO4)3和MgCl2的混合溶液,向其中逐滴加入NaOH溶液,得到沉淀的物质的量(W)与加入NaOH溶液的体积关系如图所示,则原溶液中SO42-与Cl-的物质的量之比为( )
现有Al2(SO4)3和MgCl2的混合溶液,向其中逐滴加入NaOH溶液,得到沉淀的物质的量(W)与加入NaOH溶液的体积关系如图所示,则原溶液中SO42-与Cl-的物质的量之比为( )| A、1:1 | B、3:2 |
| C、2:3 | D、2:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 外,还有
外,还有 ,n个
,n个 ,其余为-OH,则-OH的个数为
,其余为-OH,则-OH的个数为查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、第四周期第ⅡA族 |
| B、第五周期第ⅣB族 |
| C、第五周期第IVA族 |
| D、第五周期第ⅡA族 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com