
(10分)自然界中的物质多数是以混合物的形式存在,下面是混合物的分离和提纯要求,请填空:
(1)除去NaCl中的Na2SO4,依次加入的溶液为(填溶质化学式):______、______、________;
(2)如图是常用的实验仪器(铁架台和玻璃导管、橡皮管、瓶塞等略去)
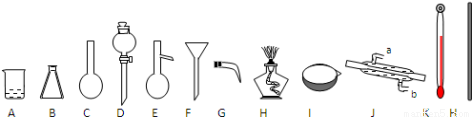
①填写以下仪器的名称:D ,J ;
②用四氯化碳萃取溴水中Br2单质,萃取能否用酒精代替四氯化碳进行实验? ,解释其原因 ;
③蒸馏装置中,在E中加入沸石的目的是 ,仪器J的冷凝水应该 进 出(填写a、b)。
(1)BaCl2、 Na2CO3、 HCl;
(2)①分液漏斗,冷凝管;②不能,水与酒精互溶;③防止液体暴沸;b、a
【解析】
试题解析:(1)Na2SO4可与BaCl2反应生成BaSO4沉淀,除去NaCl中的Na2SO4,先加入BaCl2除掉SO42-离子,再加入Na2CO3除掉过量的BaCl2,最后用HCl除掉过量的Na2CO3,得到纯净的氯化钠,故答案为:BaCl2;Na2CO3;HCl;(2)①D为分液漏斗,G为冷凝管;②乙醇不能代替四氯化碳,因为乙醇和水混溶,不能用作萃取剂;③ 蒸馏装置中,在E中加入沸石的目的是防止液体暴沸;蒸馏时,冷凝水从下端进入,从上端流出,即应该b进a出。
考点:物质的分离、提纯


科目:高中化学 来源: 题型:
| A、二氧化氮和二氧化碳 | B、一氧化碳和二氧化碳 | C、二氧化硫和二氧化碳 | D、二氧化硫和二氧化氮 |
查看答案和解析>>
科目:高中化学 来源:2015届广东省韶关市十校高三10月联考化学试卷(解析版) 题型:填空题
(16分)香豆素是用途广泛的香料,合成香豆素的路线如下(其他试剂、产物及反应条件均省略):
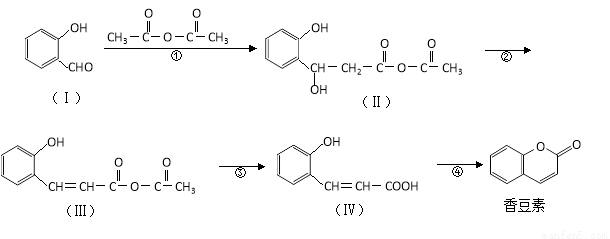
(1)香豆素的分子式为_______;Ⅰ与H2反应生成邻羟基苯甲醇,邻羟基苯甲醇的结构简式为______。
(2)反应②的反应类型是_____________,反应④的反应类型是_____________。
(3)香豆素在过量NaOH溶液中完全水解的化学方程式为_______________。
(4)Ⅴ是Ⅳ的同分异构体,Ⅴ的分子中含有苯环且无碳碳双键,苯环上含有两个邻位取代基,能发生银镜反应。Ⅴ的结构简式为_______________(任写一种)。
(5)一定条件下, 与CH3CHO能发生类似反应①、②的两步反应,最终生成的有机物
与CH3CHO能发生类似反应①、②的两步反应,最终生成的有机物
的结构简式为_____________。
查看答案和解析>>
科目:高中化学 来源:2015届广东省湛江市高三第一次月考理综化学试卷(解析版) 题型:选择题
常温下,往H2O2溶液中滴加少量FeSO4溶液,可发生如下两个反应:
2Fe2++H2O2+2H+=2Fe3++2H2O 2Fe3++H2O2=2Fe2++O2↑+2H+下列说法不正确的是
A.H2O2的氧化性比Fe3+强,其还原性比Fe2+强
B.在H2O2分解过程中, Fe2+和Fe3+的总量保持不变
C. 在H2O2分解过程中,溶液的pH逐渐下降
D.H2O2生产过程要严格避免混入Fe2+
查看答案和解析>>
科目:高中化学 来源:2015届广东省湛江市高一第一学期期中考试化学试卷(解析版) 题型:选择题
海带中含碘元素,从海带中提取碘有如下步骤:
①通入足量Cl2 ②将海带焙烧成灰后加水搅拌 ③加CCl4振荡
④用分液漏斗分液 ⑤过滤
合理的操作顺序是
A.②⑤①③④ B.①②③④⑤ C.②①③⑤④ D.①③⑤②④
查看答案和解析>>
科目:高中化学 来源:2015届江苏省盐城市、建湖二中高一上学期期中联考化学试卷(解析版) 题型:选择题
用NA表示阿伏加德罗常数的值,下列说法正确的是
A、16g O2中含有的氧分子数为NA
B、1mol Zn变为Zn2+时失去的电子数目为NA
C、常温常压下,11.2 L H2中含有的氢分子数为0.5NA
D、1L 1 mol·L-1 BaCl2溶液中含有的钡离子数为NA
查看答案和解析>>
科目:高中化学 来源:2015届江苏省盐城市、建湖二中高一上学期期中联考化学试卷(解析版) 题型:选择题
同温、同压下,决定气体体积的主要因素是
A、气体分子的直径 B、气体的分子数目
C、气体分子间的平均距离 D、气体分子的摩尔质量
查看答案和解析>>
科目:高中化学 来源:2015届江苏省淮安市高三上学期第一次阶段性测试化学试卷(解析版) 题型:选择题
温度为T时,向2.0 L恒容密闭容器中充入2.0 mol NO2,反应2NO2(g) N2O4(g)经一段时间后达到平衡。反应过程中测定的部分数据见下表:
N2O4(g)经一段时间后达到平衡。反应过程中测定的部分数据见下表:
t/s | 0 | 50 | 150 | 250 | 350 |
n(N2O4)/mol | 0 | 0.12 | 0.18 | 0.20 | 0.20 |
下列说法正确的是
A.反应在前50 s的平均速率为v(NO2)=0.001 2 mol·L-1·s-1
B.保持温度不变,向平衡后的容器中充入1.0 mol N2O4时,v(正)<v(逆)
C.保持其他条件不变,升高温度达到新平衡时K=0.125,则反应的ΔH<0
D.T温度时,若起始向容器中充入2.0 mol N2O4,则平衡时N2O4的转化率大于80%
查看答案和解析>>
科目:高中化学 来源:2015届江苏省泰州市姜堰区高二上学期中考试化学试卷(选修)(解析版) 题型:填空题
(16分)化学反应原理对化学反应的研究具有指导意义。
(1)机动车废气排放已成为城市大气污染的重要来源。
①气缸中生成NO的反应为:N2(g)+O2(g)  2NO(g) △H >0。汽车启动后,气缸内温度越高,单位时间内NO排放量越大,请分析两点原因 、 。
2NO(g) △H >0。汽车启动后,气缸内温度越高,单位时间内NO排放量越大,请分析两点原因 、 。
②汽车汽油不完全燃烧时还产生CO,若设想按下列反应除去CO:
2CO(g)=2C(s)+O2(g) ΔH>0,该设想能否实现? (选填“能”或“不能”),依据是 。
(2)氯气在298K、100kPa时,在1L水中可溶解0.09mol,实验测得溶于水的Cl2约有1/3与水反应。该反应的离子方程式为 ,在上述平衡体系中加入少量NaOH固体,溶液中Cl—浓度 (选填“增大”、“减小”或“不变”)。
(3)一定条件下,Fe3+和I—在水溶液中的反应是2I—+2Fe3+ I2+2Fe2+,当反应达到平衡后,加入CCl4充分振荡,且温度不变,上述平衡向 (选填“正反应”或“逆反应”)方向移动。请设计一种使该反应的化学平衡逆向移动的实验方案 。
I2+2Fe2+,当反应达到平衡后,加入CCl4充分振荡,且温度不变,上述平衡向 (选填“正反应”或“逆反应”)方向移动。请设计一种使该反应的化学平衡逆向移动的实验方案 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com