
【题目】下列说法中正确的是
A.铁的摩尔质量就是铁的相对原了质量 B.CO32-的摩尔质量是60g/mol
C.1molO2的质量是32g/mol D.标准状况下,18g水的体积是22.4L
 高中必刷题系列答案
高中必刷题系列答案科目:高中化学 来源: 题型:
【题目】有关水解原理的应用,下列说法正确的是
A.将NaHCO3溶液蒸干并灼烧时,HCO3-+H2O![]() H2CO3+OH-向正向移动,最后可以得到NaOH固体
H2CO3+OH-向正向移动,最后可以得到NaOH固体
B.MgSO4酸性溶液中含有杂质离子Fe2+时,可以先加人氯水将Fe2+氧化成Fe3+,再加入MgO除去杂质
C.为抑制离子的水解,在配制SnCl2溶液时,可以加入适量稀硫酸加以酸化
D.用MgCl2 6H2O制取无水MgCl2时,需要在HCl气流中加热
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数的值,下列说法中正确的是
A. ![]() 的NH4NO3溶液中氮原子数小于0.2NA
的NH4NO3溶液中氮原子数小于0.2NA
B. 某温度时,1LpH=6的纯水中含有1.0X10-6NA个OH-
C. 在O2参加的反应中,1mol O2作氧化剂时得到的电子数一定是4NA
D. 向含有0.4 mol FeBr2的溶液中通入0.3 mol Cl2,充分反应时转移的电子数为1.2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组元素性质的递变情况错误的是( )
A.Li、Be、B原子最外层电子数依次增多
B.P、S、C1元素最高正价依次升高
C.N、O、F原子半径依次增大
D.Na、K、Rb的电子层数依次增多
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铝与过量的稀盐酸反应,为了加快反应速率,但是又不影响生成的氢气总量,可以采取的措施是( )
A. 加入适量的铝粉 B. 加入适量的水
C. 加入少量的硫酸铜溶液 D. 加入浓度较大的盐酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物A的红外光谱和核磁共振氢谱如下图所示,下列说法中错误的是( )

A. 由红外光谱可知,该有机物中至少含有三种不同的化学键
B. 由核磁共振氢谱可知,该有机物分子中有三种不同的氢原子
C. 若A的化学式为C2H6O,则其结构简式为CH3-O-CH3
D. 仅由其核磁共振氢谱无法得知其分子中的氢原子总数
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A、B、C、D、E、F是中学化学中常见的六中有机物,它们的转化关系如图1所示(部分物质已省略).其中A是一种生物生长调节剂,E具有水果香味,F是一种可制成多种包装材料的高分子化合物。

(1)C的结构简式为____。
(2)D分子中官能团的名称____,证明该官能团具有酸性的方法为 。
(3)写出图1转化过程中的化学反应方程式① ____;② ;⑤ 。
(4)写出图1有机反应类型① ______ ;② ______。
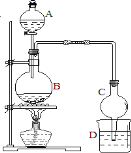
(5) 某课外小组设计的实验室制取乙酸乙酯的装置如图2所示,A中放有浓硫酸,B中放有乙醇、醋酸,D中放有饱和碳酸钠溶液.请回答:
①浓硫酸的作用是______;
②若用同位素 18O标记乙醇中的氧原子,则CH 3CH 2 18OH与乙酸生成乙酸乙酯的化学方程式为____。
③球形干燥管C的作用是 。
④反应结束后D中的现象 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作中错误的是( )
A. 蒸馏实验时,在烧瓶内加几粒沸石以防止暴沸
B. 制蒸馏水时,应使温度计水银球靠近蒸馆烧瓶的支管口处
C. 分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出
D. 进行过滤时,玻璃棒的末端应轻轻靠在三层的滤纸上
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业废水中常含有一定量Cr2O72-和CrO42-,它们会对人类及生态系统产生很大伤害。
已知:i. 2CrO42-(黄色)+ 2H+ ![]() Cr2O72-(橙色)+ H2O
Cr2O72-(橙色)+ H2O
ii. Cr(OH)3(s) + H2O ![]() [Cr(OH)4]- (亮绿色) + H+
[Cr(OH)4]- (亮绿色) + H+
(1) 含铬工业废水的一种处理流程如下:
![]()
① i. 若在转化一步中调节溶液的pH=2,则溶液显_______色。
ii. 能说明转化一步反应达平衡状态的是_______(填字母序号)。
a.Cr2O72-和CrO42-的浓度相同 b.ν正(Cr2O72-) = 2ν逆(CrO42-)
c.溶液的颜色不变 d.溶液的pH不变
② 步骤②还原一步的离子方程式是___________________________;若还原l mol Cr2O72-离子,需要FeSO4·7H2O的物质的量是_______mol。
③ 沉淀一步中,向含Cr3+(紫色)溶液中,逐渐滴加NaOH溶液。当pH=4.6时,开始出现灰绿色沉淀,随着pH的升高,沉淀量增多。当pH≥13时,沉淀逐渐消失,溶液变为亮绿色。
i. 请解释溶液逐渐变为亮绿色的原因:_______。
ii. 若向0.05mol·L-1的Cr2(SO4)3溶液50mL中,一次性加入等体积0.6 mol·L-1的NaOH溶液,充分反应后,溶液中可观察到的现象是__________。
④ 在K[Cr(OH)4]和K2Cr2O7混合溶液中加入足量H2SO4酸化,铬元素以_______形式存在(填离子符号)。
(2) 用Fe做电极电解含Cr2O72-的酸性工业废水,可以直接除去铬。随着电解进行,在阴极附近溶液pH升高,产生Cr(OH)3沉淀。
① 结合上述工业流程分析用Fe做电极的原因:_______。
② 结合电极反应式解释在阴极附近溶液pH升高的原因:_______。
③ 溶液中同时生成的沉淀可能还有_______(填化学式)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com