



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
 2009��12��7��һ18���ڵ������籾�����ٿ������Ϲ�������飬��δ��Ӧ������仯��ȫ���ж�ǩ���µ�Э�飮����ν��ʹ�����CO2�ĺ�������Ч�ؿ�������CO2��������ȫ������ձ����ӣ�Ϊ��С������CO2�Ի�����Ӱ�죬һ����������������������ŷ�������һ�����ѧ�Ҽ�ǿ�˶�CO2�������õ��о���
2009��12��7��һ18���ڵ������籾�����ٿ������Ϲ�������飬��δ��Ӧ������仯��ȫ���ж�ǩ���µ�Э�飮����ν��ʹ�����CO2�ĺ�������Ч�ؿ�������CO2��������ȫ������ձ����ӣ�Ϊ��С������CO2�Ի�����Ӱ�죬һ����������������������ŷ�������һ�����ѧ�Ҽ�ǿ�˶�CO2�������õ��о���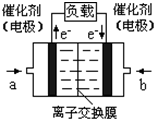 ��ͼ����a��ͨ�����
��ͼ����a��ͨ������鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
2009��12��18�շ��������������������������ҽר�ҳ���7���µĿ��й��أ������Ƴ�һ����Ч���Ƽ���H1N1���е�����ҩ������з���������Ҫ�ɷ�֮һ�ǽ�������������������Ч�ɷ�֮һ����ԭ�ᡣ�������й���ԭ��ķ��ӽṹ����ת����ϵ������EΪ���������䱽���ϵ�һ�ȴ���ֻ��һ�֣����ֲ���ʡ�ԣ�


��ش��������⣺
��1����ԭ��ķ���ʽ�� ��A�к��������ŵ�����Ϊ ��H�Ľṹ��ʽΪ ��
��2���ٵķ�Ӧ������ ��1mol��ԭ��������� molNaOH��
��3��������E��ͬ���칹�壨��E������ͬ��ȡ�������ķе��ɴ�С��˳���ǣ�����E���ڣ� ���ýṹ��ʽ��ʾ����
��4��д����Ӧ�ۡ��ܵĻ�ѧ����ʽ��
�� ��
�� ��
��5��B�ǿ����ᣬ���ж���ͬ���칹�壬д��������������������ͬ���칹��Ľṹ��ʽ����������a.�����Ϻ�������ȡ�������ұ����ϵ�һ�ȴ���ֻ�����֣�b.�ܷ���ˮ�ⷴӦ���Ҳ���֮һ�ܷ���������Ӧ��c.����̼��������Һ��Ӧ�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
��15�֣�2009��12��7��һ18���ڵ������籾�����ٿ������Ϲ�������飬��δ��Ӧ������仯��ȫ���ж�ǩ���µ�Э�顣����ν��ʹ�����CO2�ĺ�������Ч�ؿ�������CO2��������ȫ������ձ����ӡ�Ϊ��С������CO2�Ի�����Ӱ�죬һ����������������������ŷ�������һ�����ѧ�Ҽ�ǿ�˶�CO2�������õ��о���
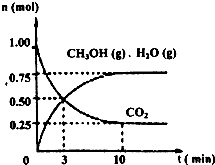
��1��Ŀǰ��ҵ����һ�ַ�������CO2������ȼ�ϼ״���Ϊ̽���÷�Ӧԭ������������ʵ�飺ij�¶��£����ݻ�Ϊ2L���ܱ������У�����1mol CO2��3��25molH2����һ�������·�����Ӧ�����CO2��CH3OH��g����H2O��g�������ʵ�����n����ʱ��仯����ͼ��ʾ��
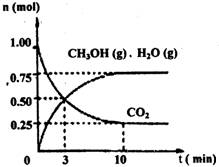
�ٴӷ�Ӧ��ʼ��ƽ�⣬������ƽ����Ӧ����v��H2��= ��
�����д�ʩ��һ������ʹn��CH3OH��/n��CO2��������ǣ� ��
A�������¶� B����С�������ݻ�
C����ˮ��������ϵ�з��� D��ʹ�ø���Ч�Ĵ���
��2�����³�ѹ�£�����CO 2ˮ��Һ��pH =5��6��c��H2CO3��=1��5 ��l0-5mol��L-1���� ����ˮ�ĵ��뼰H2CO3�ĵڶ������룬��H2CO3HCO3- +H+�ĵ���ƽ�ⳣ��K= ������֪��10 -5��6=2��5��l0-6����
��3����״���£���1��12LCO2ͨ��100mL 1mol��L-1��NaOH��Һ�У�������Һ������Ũ���ɴ�С��˳��Ϊ ��
��4����ͼ���Ҵ�ȼ�ϵ�أ��������ҺΪKOH��Һ���Ľṹʾ��ͼ����a��ͨ����� ����Ҵ���������������b���缫�Ϸ����ĵ缫��Ӧ�ǣ� ��
��5��CO2����Ȼ��ѭ��ʱ����CaCO3��Ӧ��CaCO3��һ���������ʣ���Ksp=2��8��10��9��CaCl2��Һ��Na2CO3��Һ��Ͽ��γ�CaCO3�������ֽ��������CaCl2��Һ��Na2CO3��Һ��ϣ���Na2CO3��Һ��Ũ��Ϊ2��10��4mo1/L �������ɳ�������CaCl2��Һ����СŨ��Ϊ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2011�����ʡ�Ƹ�������һ�и߿���ѧģ���Ծ��������棩 ���ͣ�ѡ����
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com