
·ÖĪö £Ø1£©A”¢B”¢CŹĒµŚ¶žÖÜĘŚµÄ·Ē½šŹōŌŖĖŲ£¬ĘäŌ×ÓŠņŹżŅĄ“ĪŌö“ó£¬ĖüĆĒµÄŌ×ÓŠņŹżŅĄ“ĪŌö“ó£¬ĖüĆĒÖ®¼äæÉŅŌŠĪ³ÉACŗĶBCŅŌ¼°AC2ŗĶBC2·Ö×Ó£¬ŌņAĪŖC”¢BĪŖN”¢CĪŖO£»DŌŖĖŲŹĒŅ»ÖÖ¶ĢÖÜĘŚŌŖĖŲ£¬ĖüÓėA”¢B”¢CæÉ·Ö±šŠĪ³Éµē×Ó×ÜŹżĻąµČµÄČżÖÖ·Ö×Ó£¬ŌņDĪŖHŌŖĖŲ£»
£Ø2£©¹¤ŅµÉś²śÖŠNH3ÓėŃõĘųŌŚ“߻ƼĮĢõ¼žĻĀ·“Ӧɜ³ÉNOÓėĖ®£»
£Ø3£©·“Ó¦ÖŠÖ»ÓŠNŌŖĖŲ»ÆŗĻ¼ŪµÄÉżøߣ¬¶ųƻӊŌŖĖŲ»ÆŗĻ¼ŪµÄ½µµĶ£¬·“Ó¦²»ÄÜ·¢Éś£»
£Ø4£©ÓÉA”¢C”¢DČżÖÖŌŖĖŲ×é³ÉµÄ»ÆŗĻĪļA2D6CĪŖC2H5OH£¬ŌŚŅ»¶ØĢõ¼žĻĀæÉŅŌ×Ŗ»ÆĪŖCH3CHO£¬ŹµĻÖøĆ×Ŗ»ÆµÄ»Æѧ·½³ĢŹ½ĪŖ£ŗ2C2H5OH+O2$”ś_{”÷}^{“߻ƼĮ}$2CH3CHO+2H2O£»
£Ø5£©¢Łøł¾Ż·½³ĢŹ½æÉÖŖ£¬AC2ŗĶB2µÄĪļÖŹµÄĮæÖ®±ČĪŖ4£ŗ1£¬¹ŹÉś³ÉB2¹²ĪŖ0.2a mol£¬øł¾Ż·½³ĢŹ½¼ĘĖć²Ī¼Ó·“Ó¦µÄACµÄĪļÖŹµÄĮ棬ŌŁøł¾Ż×Ŗ»ÆĀŹ¶ØŅå¼ĘĖć£»
¢ŚÓÉ¢ŁÖŠĪŖŗćĪĀŗćŃ¹£¬¢ŚÖŠĪŖŗćĪĀŗćČŻ£¬Ėę·“Ó¦½ųŠŠŃ¹Ēæ½µµĶ£¬Ļąµ±ÓŚŌŚ¢ŁµÄ»ł“”ÉĻ½µµĶŃ¹Ē棬·“Ó¦ĪļµÄ×Ŗ»ÆĀŹ½µµĶ£¬¾Ż“ĖÅŠ¶Ļ£®
½ā“š ½ā£ŗ£Ø1£©A”¢B”¢CŹĒµŚ¶žÖÜĘŚµÄ·Ē½šŹōŌŖĖŲ£¬ĘäŌ×ÓŠņŹżŅĄ“ĪŌö“ó£¬ĖüĆĒµÄŌ×ÓŠņŹżŅĄ“ĪŌö“ó£¬ĖüĆĒÖ®¼äæÉŅŌŠĪ³ÉACŗĶBCŅŌ¼°AC2ŗĶBC2·Ö×Ó£¬ŌņAĪŖC”¢BĪŖN”¢CĪŖO£»DŌŖĖŲŹĒŅ»ÖÖ¶ĢÖÜĘŚŌŖĖŲ£¬ĖüÓėA”¢B”¢CæÉ·Ö±šŠĪ³Éµē×Ó×ÜŹżĻąµČµÄČżÖÖ·Ö×Ó£¬ŌņDĪŖHŌŖĖŲ£¬
¹Ź“š°øĪŖ£ŗC£»N£»O£»H£»
£Ø2£©¹¤ŅµÉś²śÖŠNH3ÓėŃõĘųŌŚ“߻ƼĮĢõ¼žĻĀ·“Ӧɜ³ÉNOÓėĖ®£¬·“Ó¦·½³ĢŹ½ĪŖ£ŗ4NH3+5O2$\frac{\underline{“߻ƼĮ}}{”÷}$4NO+6H2O£¬
¹Ź“š°øĪŖ£ŗ4NH3+5O2$\frac{\underline{“߻ƼĮ}}{”÷}$4NO+6H2O£»
£Ø3£©·“Ó¦ÖŠÖ»ÓŠNŌŖĖŲ»ÆŗĻ¼ŪµÄÉżøߣ¬¶ųƻӊŌŖĖŲ»ÆŗĻ¼ŪµÄ½µµĶ£¬·“Ó¦²»ÄÜ·¢Éś£¬
¹Ź“š°øĪŖ£ŗ²»ÄÜ£»·“Ó¦ÖŠÖ»ÓŠNŌŖĖŲ»ÆŗĻ¼ŪµÄÉżøߣ¬¶ųƻӊŌŖĖŲ»ÆŗĻ¼ŪµÄ½µµĶ£»
£Ø4£©ÓÉA”¢C”¢DČżÖÖŌŖĖŲ×é³ÉµÄ»ÆŗĻĪļA2D6CĪŖC2H5OH£¬ŌŚŅ»¶ØĢõ¼žĻĀæÉŅŌ×Ŗ»ÆĪŖCH3CHO£¬ŹµĻÖøĆ×Ŗ»ÆµÄ»Æѧ·½³ĢŹ½ĪŖ£ŗ2C2H5OH+O2$”ś_{”÷}^{“߻ƼĮ}$2CH3CHO+2H2O£¬
¹Ź“š°øĪŖ£ŗ2C2H5OH+O2$”ś_{”÷}^{“߻ƼĮ}$2CH3CHO+2H2O£»
£Ø5£©¢Łøł¾Ż·½³ĢŹ½æÉÖŖ£¬AC2ŗĶB2µÄĪļÖŹµÄĮæÖ®±ČĪŖ4£ŗ1£¬¹ŹÉś³ÉB2¹²ĪŖamol”Į$\frac{1}{5}$=0.2a mol£¬øł¾Ż·½³ĢŹ½æÉÖŖ²Ī¼Ó·“Ó¦µÄACµÄĪļÖŹµÄĮæĪŖ4”Į0.2amol=0.8 amol£¬¹ŹACµÄ×Ŗ»ÆĀŹĪŖ$\frac{0.8amol}{1mol}$”Į100%=80a%£¬
¹Ź“š°øĪŖ£ŗ80a%£»
¢ŚÓÉ¢ŁÖŠĪŖŗćĪĀŗćŃ¹£¬¢ŚÖŠĪŖŗćĪĀŗćČŻ£¬Ėę·“Ó¦½ųŠŠŃ¹Ēæ½µµĶ£¬Ļąµ±ÓŚŌŚ¢ŁµÄ»ł“”ÉĻ½µµĶŃ¹Ēæ£¬Ę½ŗāĻņÄę·“Ó¦·½ĻņŅĘ¶Æ£¬·“Ó¦ĪļµÄ×Ŗ»ÆĀŹ½µµĶ£¬¹ŹÉś³É³ÉAC2ŗĶB2µÄĪļÖŹµÄĮæ¼õŠ”£¬¹Źa£¾b£¬¹Ź“š°øĪŖ£ŗ£¾£®
µćĘĄ ±¾Ģāæ¼²éŌŖĖŲĶʶĻ”¢Ńõ»Æ»¹Ō·“Ó¦”¢»ÆŃ§Ę½ŗāÓŠ¹Ų¼ĘĖćµČ£¬ÄѶČÖŠµČ£¬ĶʶĻŌŖĖŲŹĒ½āĢā¹Ų¼ü£¬ŠčŅŖѧɜ¶ŌŌŖĖŲ»ÆŗĻĪļÖŖŹ¶ŹģĮ·ÕĘĪÕ£¬£Ø5£©ÖŠ¢Ś×¢ŅāĄūÓƵȊ§Ė¼Ļė¹¹½ØĘ½ŗā½ØĮ¢µÄĶ¾¾¶½ųŠŠ±Č½Ļ£®


 ĢģĢģĻņÉĻŅ»±¾ŗĆ¾ķĻµĮŠ“š°ø
ĢģĢģĻņÉĻŅ»±¾ŗĆ¾ķĻµĮŠ“š°ø Š”ѧɜ10·ÖÖÓÓ¦ÓĆĢāĻµĮŠ“š°ø
Š”ѧɜ10·ÖÖÓÓ¦ÓĆĢāĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | NH4+”¢Cl-”¢K+”¢SO42- | B£® | Fe3+”¢Na+”¢OH-”¢NO3- | ||
| C£® | Ag+”¢Na+”¢Cl-”¢NO3- | D£® | H+”¢Na+”¢NO3-”¢CO32- |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¹čŹĒČĖĄą½«Ģ«ŃōÄÜ×Ŗ»»ĪŖµēÄܵij£ÓĆ²ÄĮĻ | |
| B£® | “Ö¹čÖʱøµ„¾§¹č²»Éę¼°Ńõ»Æ»¹Ō·“Ó¦ | |
| C£® | Ė®Äą”¢Ė®¾§ŗĶ²ĶץÉĻµÄ“ÉÅĢ¶¼ŹĒ¹čĖįŃĪÖĘĘ· | |
| D£® | ŃĪĖįæÉŅŌÓė¹č·“Ó¦£¬¹Ź²ÉÓĆŃĪĖįĪŖÅ×¹āŅŗÅ×¹āµ„¾§¹č |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 ijĪĀ¶Č£Øt”ę£©ĻĀµÄČÜŅŗÖŠ£¬c£ØH+£©=10-x mol/L£¬c£ØOH-£©=10-y mol/L£¬xÓėyµÄ¹ŲĻµČēĶ¼ĖłŹ¾£®Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
ijĪĀ¶Č£Øt”ę£©ĻĀµÄČÜŅŗÖŠ£¬c£ØH+£©=10-x mol/L£¬c£ØOH-£©=10-y mol/L£¬xÓėyµÄ¹ŲĻµČēĶ¼ĖłŹ¾£®Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
| Ąė×ÓÅØ¶Č“Ó“óµ½Š”µÄĖ³Šņ | ČÜÖŹ»ÆѧŹ½ | ČÜŅŗµÄpHÖµ |
| c£ØNH4+£©£¾c£ØOH-£©£¾c£ØCl-£©£¾c£ØH+£© | NH4Cl”¢NH3£®H2O | £¾7 |
| c£ØNH4+£©=c£ØCl-£©£¾c£ØH+£©=c£ØOH-£© | NH4Cl”¢NH3£®H2O | =7 |
c£ØCl-£©£¾c£ØNH4+£©£¾c£ØH+£©£¾c£ØOH-£© | NH4Cl | £¼7 |
| c£ØCl-£©£¾c£ØH+£©£¾c£ØNH4+£©£¾c£ØOH-£© | NH4Cl HCl | £¼7 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
 ¢ŪCH3CH2Br¢Ü
¢ŪCH3CH2Br¢Ü ¢Ż
¢Ż ¢Ž
¢Ž ¢ß
¢ß ¢ą
¢ą ¢į
¢į ¢ā
¢ā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 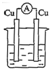 Ļ”ĮņĖį | B£® | 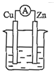 Ļ”ĮņĖį | C£® | 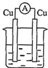 ¾Ę¾« | D£® | 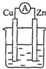 ZnSO4 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ö¬·¾ | B£® | µķ·Ū | C£® | µ°°×ÖŹ | D£® | °±»łĖį |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā

| A£® | ×ŌČ¼ĪļĘ·”¢Ņ×Č¼ | B£® | øÆŹ“ŠŌ”¢ÓŠ¶¾ | C£® | ±¬ÕØŠŌ”¢øÆŹ“ŠŌ | D£® | Ńõ»Æ¼Į”¢ÓŠ¶¾ |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com