
| A. | 电子从3s能级跃迁到3p能级形成的光谱是发射光谱 | |
| B. | 白磷(P4)分子是正四面体结构,故分子中的键角为109°28′ | |
| C. | NO2- 中心原子采取sp2杂化,分子空间构型为“V”形 | |
| D. | 原子晶体熔点不一定比金属晶体高,分子晶体熔点不一定比金属晶体低 |
分析 A.电子从3S能级跃迁到3P能级要吸收能量;
B.白磷(P4)分子中键角为60°;
C.根据中心原子的价层电子对数判断;
D.根据二氧化硅、钨、碘、汞的熔点,举例分析.
解答 解:A.3s轨道的能量低于3p轨道的能量,所以电子从3s能级跃迁到3p能级要吸收能量,形成的光谱是吸收光谱,故A错误;
B.白磷(P4)分子是正四面体结构,白磷(P4)分子中键角为60°,不是为109°28′;故B错误;
C.NO2- 中心原子的价层电子对数=2+$\frac{1}{2}$(5+1-2×2)=3,采取sp2杂化,含有一个孤电子对,分子空间构型为“V”形,故C正确;
D.原子晶体熔点不一定比金属晶体高,如熔点SiO2<W,分子晶体熔点不一定比金属晶体低,如熔点I2>Hg,故D正确.
故答案为:CD.
点评 本题考查较为综合,涉及原子轨道、键角、杂化理论的应用以及熔沸点比较等问题,侧重于学生的分析能力和对基础知识的应用能力的考查,注意把握杂化理论的应用以及晶体熔点的比较方法.


科目:高中化学 来源: 题型:实验题
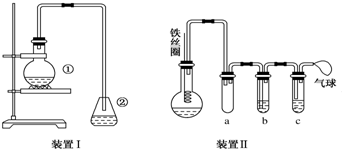
 .②中离子方程式为Br-+Ag+═AgBr↓.
.②中离子方程式为Br-+Ag+═AgBr↓. 与Br2,要想得到纯净的产物,可用NaOH溶液试剂洗涤.洗涤后分离粗产品应使用的仪器是分液漏斗.
与Br2,要想得到纯净的产物,可用NaOH溶液试剂洗涤.洗涤后分离粗产品应使用的仪器是分液漏斗.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温时不能发生的过程都是非自发过程 | |
| B. | 体系的无序性越高,即混乱度越高,熵值就越大 | |
| C. | 所有自发进行的化学反应都是放热反应 | |
| D. | 同一物质的固、液、气三种状态的熵值相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 已知2C(s)+O2(g)=2CO(g)△H=-221 kJ•mol-1,则可知C的标准燃烧热为110.5 kJ•mol-1 | |
| B. | 在101KPa下氢气的标准燃烧热△H=-285.5 kJ•mol-1,则水分解的热化学方程式:2H2O(l)=2H2(g)+O2(g)△H=+285.5 kJ•mol-1 | |
| C. | 稀硫酸与0.1 mol/LNaOH溶液反应:H+(aq)+OH-(aq)=H2O(l)△H=-57.3 kJ•mol-1 | |
| D. | 密闭容器中,9.6 g硫粉与11.2 g铁粉混合加热生成硫化亚铁17.6 g时,放出19.12 kJ热量.则Fe(s)+S(g)=FeS(s)△H=-95.6 kJ•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用激光笔检验豆浆的丁达尔现象 | |
| B. | 胶体的分散质粒子直径小于l00nm但大于1nm,能通过滤纸,不能透过半透膜 | |
| C. | 存在自由移动的离子是电解质溶液导电的原因 | |
| D. | 用萃取的方法分离汽油和煤油 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②④ | B. | ①③④ | C. | ②③④ | D. | ①②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com