
����Ŀ�������£���a mol N2��b mol H2�Ļ������ͨ��һ���̶��ݻ�Ϊ2L���ܱ������У��������·�Ӧ��N2+ 3H2 ![]() 2NH3��
2NH3��
��1������Ӧ����5minʱ�����n(N2) = 1.8mol��n(NH3) = 0.4mol��
���㣺��a��ֵ�� ����H2Ũ�ȵı仯��ʾ�ķ�Ӧ���ʡ�
��2����Ӧ��ƽ��ʱ���������������ʵ���Ϊ5.0mol������NH3�ĺ��������������Ϊ40%��
���㣺�����¶��¸÷�Ӧ�Ļ�ѧƽ�ⳣ����
���𰸡���1����2 ��0.06 mol/(L��min) ��2��2
��������
������1�� N2 + 3H2 ![]() 2NH3
2NH3
��ʼ���ʵ��� a b 0
�仯���ʵ��� 0.2 0.6 0.4
5minʱ���ʵ��� 1.8 b-0.6 0.4
a=0.2+1.8=2 ������Ũ�ȵı仯��ʾ�ķ�Ӧ����Ϊv (H2)=0.6mol��(2L��5min)=0.06 mol/(L��min)
��2�� N2 + 3H2 ![]() 2NH3
2NH3
��ʼ���ʵ��� 2 b 0
�仯���ʵ��� 1 3 2
ƽ�����ʵ��� 1 b-3 2
1+2+b-3=5 ���b=5 K=��1��1���£�0.5��13��=2



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������仯������NH3����Ρ�N2H4��N2O4������ѧ��ѧ��������ҵ������������ռ����Ҫ��λ��
(1)���亽����������(N2H4)��N2O4��ȼ������ȼ������(N2H4)��N2O4�ķ�ӦΪ
2N2H4 (g)+ N2O4(g)==3N2(g)+4H2O(g) ��H=-1077 kJ��mol-1��
��֪��ط�Ӧ�Ļ�ѧ�������������±���ʾ��
��ѧ�� | N��H | N��N |
| O��H |
E/(kJ��mol��1) | 390 | 190 | 946 | 460 |
��ʹ1 mol N2O4(g)�����л�ѧ����ȫ����ʱ��Ҫ���յ�������________________��
��������˵��2N2H4 (g)+ N2O4(g)==3N2(g)+4H2O(g) ��H ��ƽ��״̬����________
a.��������ƽ����Է����������� b.V��N2��=3V�� N2O4��
c.N2H4���������ֲ��� d. ��H���ٱ仯
(2)N2O4��NO2֮����ڷ�ӦN2O4(g) ![]() 2NO2(g)����һ������N2O4���˺����ܱ������У������ƽ��ת����[��(N2O4)]���¶ȵı仯����ͼ��ʾ��
2NO2(g)����һ������N2O4���˺����ܱ������У������ƽ��ת����[��(N2O4)]���¶ȵı仯����ͼ��ʾ��

����ͼ�Ʋ�÷�Ӧ�ġ�H_______0(��>����<��)������Ϊ____________________________��
��ͼ��a���Ӧ�¶��£���֪N2O4����ʼѹǿp0Ϊ108 kPa������¶��·�Ӧ��ƽ�ⳣ��Kp��________________ (��ƽ���ѹ����ƽ��Ũ�ȼ��㣬��ѹ=��ѹ�����ʵ�������)��
(3)���NO2�Ʊ�NH4NO3���乤��ԭ������ͼ��ʾ��

�������ĵ缫��ӦʽΪ____________________________________________________��
��Ϊʹ������ȫ��ת��ΪNH4NO3���貹��ij�ֻ����������A����A�Ļ�ѧʽΪ________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и�������ȷ������ ��
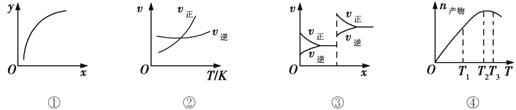
A. ͼ����ʾ�ں���������MgSO4(s) + CO(g)![]() MgO(s) + CO2(g) + SO2(g)���������������þ��������������ɴ���CO��ת����
MgO(s) + CO2(g) + SO2(g)���������������þ��������������ɴ���CO��ת����
B. ͼ����ʾ��������һ��ʱ����ӦA(g)+3B(g)![]() 2C(g)�ķ�Ӧ�������¶ȱ仯��ͼ������Ӧ��H>0
2C(g)�ķ�Ӧ�������¶ȱ仯��ͼ������Ӧ��H>0
C. ͼ����Ӧ�ķ�Ӧһ���Ƿǵ������Ӧ��ѹ��ƽ���ƶ��ı仯���
D. ��ѹ�ܱ������м���һ����A��B��������ӦA(g)+3B(g)![]() 2C(g)��ͼ����ʾ��Ӧ�����в��������¶ȣ�����C���ʵ����仯���ɣ�������Ӧ��������
2C(g)��ͼ����ʾ��Ӧ�����в��������¶ȣ�����C���ʵ����仯���ɣ�������Ӧ��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������л���![]()
![]() ��˵����ȷ����
��˵����ȷ����
A. a��b��Ϊͬϵ��
B. c������̼ԭ�ӿ��ܴ���ͬһƽ��
C. a��b��c����ʹ���Ը��������Һ��ɫ
D. b��ͬ���칹���к����Ȼ��Ľṹ����7��(���������칹)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ļױ��ӵ������п��Ը������͵Ŀ������ܡ����Ҫʹ�ױ���ȫȼ�գ��ױ�����������������Ӧ��ԼΪ
A�� 1��9 B�� 1��11 C��1��26 D�� 1��45
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij������A���Դ�ú����õ���ú�����з����������AΪԭ�Ͽ��Ժϳɾ��ڰ��������ᡢ����������ʣ���ϳ���������(���ֲ���ϳ�·�ߡ���Ӧ��������ȥ)��
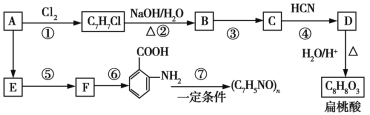
��֪��
��R��CHO+HCN![]()
![]()
��R��CN![]() R��COOH
R��COOH
��![]()
![]()
![]() (�����ױ�����)
(�����ױ�����)
��ش��������⣺
(1)C�ķ���ʽΪ__________��
(2)���ж���ط�Ӧ���͵��жϺ�������__________ (�����)��
�� | �� | �� | �� | �� | �� | �� | |
�� | �ӳ� | ˮ�� | ��ԭ | ȡ�� | ��ԭ | ���� | �Ӿ� |
�� | �ӳ� | ��ȥ | ��ԭ | �ӳ� | ���� | ��ԭ | ���� |
�� | ȡ�� | ˮ�� | �ӳ� | ���� | ��ԭ | ���� | |
�� | ȡ�� | ��ȥ | ���� | ȡ�� | ��ԭ | ���� | �Ӿ� |
(3)д����Ӧ�۵Ļ�ѧ����ʽ��______________________________��
(4)�������ж���ͬ���칹�壬���м������Ȼ�����Һ������ɫ��Ӧ��������̼��������Һ��Ӧ�������ݵ�ͬ���칹����__________�֣�д������һ�ֵĽṹ��ʽ��__________________��
(5)�Է�����AΪ��Ҫԭ�ϣ�������ͨ�����кϳ�·�ߺϳɰ�˾ƥ�ֺͶ����ͣ�

�ٶ����͵Ľṹ��ʽΪ____________________��
��д����Ӧ���Ļ�ѧ����ʽ��______________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������У��Է�������Һ����������μӵķ�Ӧ�����ʲ���������Ӱ�����( )
A. Ũ��B. ѹǿC. �¶�D. ��Ӧ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������װ���ܴﵽʵ��Ŀ�ĵ���
ѡ�� | A | B | C | D |
ʵ��װ�� |
|
|
|
|
ʵ��Ŀ�� | ̽��Na2CO3��NaHCO3�ܽ�ȵ���Դ�С | ����֪Ũ�ȵ�NaOH��Һ�ζ�δ֪Ũ�ȵ�ϡ���� | ����������Ũ���ᷴӦ������CO2 | ��֤þ��ϡ����ķ�Ӧ����ЧӦ |
A. A B. B C. C D. D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ҺΪ����ij���صķ�ӦΪFe+NiO2+2H2O Fe(OH)2+Ni(OH)2
Fe(OH)2+Ni(OH)2
��1�������س��ʱ��������ԭ��Ӧ��������_______________(��ѡ����ĸ)���ŵ�ʱ����Fe(OH)2������Ϊ18 g�������·��ת�Ƶĵ�������________________��
A��NiO2 B��Fe C��Fe(OH)2 D��Ni(OH)2
��2��Ϊ��ֹԶ���ִ��ĸ��������ں�ˮ�з����绯ѧ��ʴ��ͨ���ڴ�������ǶZn�飬 ��������ص�__________(���������)���������õ绯ѧ��������Ϊ___________________��
��3�������طŵ�ʱ�����缫��Ӧʽ__________________�����ʱ�����缫��Ӧʽ_______
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com