
pH值为4.5的盐酸1mL稀释为约1L,稀释前后溶液对指示剂的颜色变化影响是( )
A.稀释前后酚酞均为无色
B.石蕊由红色变为紫色
C.甲基橙由红色变为黄色
D.甲基橙由黄色变为橙色
科目:高中化学 来源:物理教研室 题型:021
A.稀释前后酚酞均为无色
B.石蕊由红色变为紫色
C.甲基橙由红色变为黄色
D.甲基橙由黄色变为橙色
查看答案和解析>>
科目:高中化学 来源:2013届湖南省高二第二次月考化学试卷 题型:选择题
已知在pH为4~5的环境中,Cu2+、Fe2+几乎不水解,而Fe3+几乎完全水解。工业上制CuCl2是将浓盐酸用蒸气加热到80℃左右,再慢慢加入粗氧化铜(含少量杂质FeO),充分搅拌使之溶解。欲除去溶液中的杂质离子,下述方法中可行的是
A. 向溶液中通入H2S使Fe2+沉淀
B.向溶液中通入Cl2,再通入NH3,调节pH值为4~5
C. 加入纯Cu将Fe2+还原为Fe
D.向溶液中通入Cl2,再加入纯净的CuO粉末调节pH值为4~5
查看答案和解析>>
科目:高中化学 来源: 题型:
制取纯净CuCl2?2H2O的生产过程是:
(1)用粗CuO(含少量铁)溶解在足量的稀盐酸里加热、过滤,得到CuCl2(含FeCl2)的溶液,经测定,溶液的PH值为3。
(2)对(1)的溶液按下列步骤进行提纯:
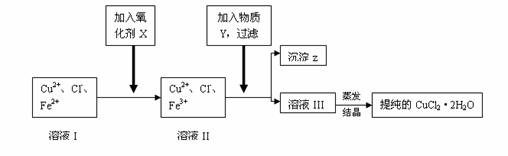
![]() 已知:①可做氧化剂的物质有(A)KMnO4 (B)K2Cr2O7 (C)H2O2 (D)NaClO
已知:①可做氧化剂的物质有(A)KMnO4 (B)K2Cr2O7 (C)H2O2 (D)NaClO
②Cu2+ 、Fe2+在PH值为4~5时不水解,而Fe3+却几乎全部水解。
试回答:
(1)加入的氧化剂X是(答编号): ;
加入X的作用是: ;
反应的离子方程式是: 。
(2)物质Y是 ;沉淀Z是 。加入Y能形成沉淀Z的原因是: 。
(3)分离出沉淀Z,并将溶液III蒸发欲获得晶体CuCl2?2H2O。采取什么措施才能顺利得到晶体CuCl2?2H2O?______________________ 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com