
分析 (1)根据用肥皂水检验硬水的方法分析;
(2)分离不溶性杂质的方法是过滤;根据反应前后原子的种类和个数不变判断;
(3)根据汗液的成分及溶液的成分分析.
解答 解:(1)检验硬水的方法是:取适量的水,向其中加肥皂水,产生的泡沫较少,则说明是硬水,故答案为:加肥皂水,产生的泡沫较少;
(2)分离不溶性杂质的方法是过滤;根据质量守恒定律反应前后原子的种类和个数不变,反应前氯原子有4个,钠原子有2个,氧原子有4个,而反应后氯化钠中钠原子有2个,氯原子有2个,所以2x中应有2个氯原子,4个氧原子,所以x的化学式为ClO2,故答案为:过滤;ClO2;
(3)人体汗液有咸味,是因为汗液中含有氯化钠,化学式为:NaCl;水在汗液中的作用是作溶剂,故答案为:NaCl;作溶剂.
点评 本题考查的是有关水的检验、除杂等于生活密切相关的问题,难度不大,依据相关的知识完成即可,注意语言的表达.


 考前必练系列答案
考前必练系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Fe2+ | B. | Fe2+、Zn2+ | C. | Fe2+、Ag+ | D. | Fe2+、Fe3+ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 完全由非金属组成的化合物不一定是共价化合物 | |
| B. | 构成分子晶体的粒子一定含有共价键 | |
| C. | 分子晶体的熔点一定比金属晶体的熔点低 | |
| D. | 含有金属离子的晶体一定是离子晶体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
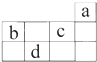
| A. | a原子的最外电子层上有8个电子 | |
| B. | c的最高价氧化物对应水化物为强酸 | |
| C. | d的原子半径比c的原子半径大 | |
| D. | b的气态氢化物比c的气态氢化物稳定 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com