
 .
.分析 A、B、C、D、E五种短周期元素,原子序数按A、B、C、D、E依次增大,原子半径按D、E、B、C、A顺序依次减小;A、D同主族,A是所有元素中原子半径最小的元素,则A为氢元素,则D为钠元素;C元素原子最外层电子数是次外层电子数的3倍,原子只能有2个电子层,最外层电子数为6,故C为氧元素;B、D、E三者的最高价氧化物对应的水化物依次为甲、乙、丙,它们两两之间均可反应生成可溶性盐和水,且所得盐中均含C元素,应是氢氧化铝与强酸、强碱之间的反应,且B与C的位置相邻,则B为氮元素、E为Al,甲为HNO3,乙为NaOH,丙为Al(OH)3;B、E两种元素原子最外层电子数之和为20,A、C、D三种元素原子最外层电子数之和为20,通过验证符合题意,据此进行答题.
解答 解:A、B、C、D、E五种短周期元素,原子序数按A、B、C、D、E依次增大,原子半径按D、E、B、C、A顺序依次减小;A、D同主族,A是所有元素中原子半径最小的元素,则A为氢元素,则D为钠元素;C元素原子最外层电子数是次外层电子数的3倍,原子只能有2个电子层,最外层电子数为6,故C为氧元素;B、D、E三者的最高价氧化物对应的水化物依次为甲、乙、丙,它们两两之间均可反应生成可溶性盐和水,且所得盐中均含C元素,应是氢氧化铝与强酸、强碱之间的反应,且B与C的位置相邻,则B为氮元素、E为Al,甲为HNO3,乙为NaOH,丙为Al(OH)3;B、E两种元素原子最外层电子数之和为20,A、C、D三种元素原子最外层电子数之和为20,符合题意,
(1)乙+丙在溶液中反应的离子方程式为:Al(OH)3+OH-=AlO2-+2H2O,
故答案为:Al(OH)3+OH-=AlO2-+2H2O;
(2)化合物NH3与NO在加热和有催化剂存在的条件下能发生反应,生成两种无毒物质,应生成氮气与水,其反应的化学方程式为:4NH3+6NO$\frac{\underline{催化剂}}{△}$5N2+6 H2O,
故答案为:4NH3+6NO$\frac{\underline{催化剂}}{△}$5N2+6H2O;
(3)D2C为Na2O,氧化钠为离子化合物,用电子式表示化合物Na2O的形成过程为: ,
,
故答案为: ;
;
(4)碳元素与元素C(原子物质的量之比1:1)形成的化合物为CO,某原电池中,电解质为KOH溶液,分别向负极通入CO,向正极通入O2,正极发生还原反应,电极反应式为:O2+4e-+2H2O=4OH-,负极发生还原反应,负极反应式为:2CO-4e-+8OH-=2CO32-+4H2O,
故答案为:O2+4e-+2H2O=4OH-;2CO-4e-+8OH-=2CO32-+4H2O.
点评 本题考查位置结构性质关系应用,题目难度中等,试题侧重对化学用语的考查,推断元素好似解题关键,注意熟练掌握原子结构与元素周期律、元素周期表的关系.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 元素代号 | 相关信息 |
| A | A的单质能与冷水剧烈反应,得到强碱性溶液 |
| B | B的原子最外层电子数是其内层电子数的三倍 |
| C | 在第3周期元素中,C的简单离子半径最小 |
| D | A、B、D组成的36电子的化合物X是常用消毒剂的主要成分 |
| E | 所有有机物中都含有E元素 |
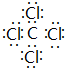 ,并写出该反应的化学方程式4Na+CCl4$\frac{\underline{\;真空高压\;}}{\;}$4NaCl+C.
,并写出该反应的化学方程式4Na+CCl4$\frac{\underline{\;真空高压\;}}{\;}$4NaCl+C.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com