

分析 (1)用海滩上的贝壳制取Ca(OH)2的反应是,碳酸钙在高温的条件下生成氧化钙和二氧化碳,氧化钙和水生成氢氧化钙;
(2)利用氢氧化钙和海水中的氯化镁反应生成氢氧化镁沉淀和氯化钙;
(3)氯化镁电解反应没意识化合价+2价变化为0价,氯元素化合价-1价变化为0价,电子转移2e-,标注双线桥法写出;
(4)氯气和氢氧化钙反应生成氯化钙、次氯酸钙和水,原子守恒配平书写化学方程式.
解答 解:(1)用海滩上的贝壳制取Ca(OH)2的反应是,碳酸钙在高温的条件下生成氧化钙和二氧化碳,氧化钙和水生成氢氧化钙,反应的化学方程式为:CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑,CaO+H2O═Ca(OH)2,
故答案为:CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑,CaO+H2O═Ca(OH)2;
(2)利用氢氧化钙和海水中的氯化镁反应生成氢氧化镁沉淀和氯化钙,反应的化学方程式为:MgCl2+Ca(OH)2═Mg(OH)2↓+CaCl2,
故答案为:MgCl2+Ca(OH)2═Mg(OH)2↓+CaCl2;
(3)氯化镁电解反应没意识化合价+2价变化为0价,氯元素化合价-1价变化为0价,电子转移2e-,标注双线桥法写出的化学方程式为: ,
,
故答案为: ;
;
(4)氯气和氢氧化钙反应生成氯化钙、次氯酸钙和水,原子守恒配平书写化学方程式,2Cl2+2 Ca(OH)2═Ca(ClO)2+CaCl2+2H2O;
故答案为:2Cl2+2 Ca(OH)2═Ca(ClO)2+CaCl2+2H2O.
点评 本题考查了海水提镁的过程分析,和步骤反应,主要是化学方程式书写方法,掌握物质性质和化学基础是解题关键,题目难度中等.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| 反应阶段 | Ⅰ | Ⅱ | Ⅲ |
| 稀盐酸体积x/mL | 0<x≤10.0 | 10.0<x≤40.0 | x>40.0 |
| 现 象 | 无气体 | 有气体 | 无气体 |
| A. | 1.00mol•L-1 | B. | 0.50mol•L-1 | C. | 1.50mol•L-1 | D. | 2.00mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | c、d、f之比可能为16:1:3 | |
| B. | 一定有a=2e,b=e | |
| C. | 若n(KClO):n(KClO3)=1:1,则a、b、c、d、e、f依次为8:4:6:1:4:1 | |
| D. | 若将该方程式拆开写成两个“半反应”,其中一定有Cl2-2e-=2Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
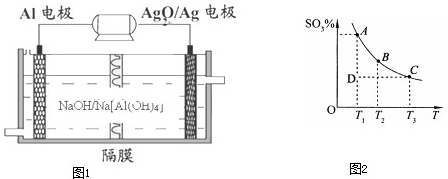
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 ,其一氯代物的结构简式是
,其一氯代物的结构简式是 ;其中一氯代物种类最多的是
;其中一氯代物种类最多的是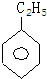 .(均填结构简式)
.(均填结构简式)查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | MgCl2+Ca(OH)2═CaCl2+Mg(OH)2↓ | B. | Mg(OH)2+2HCl═MgCl2+2H2O | ||
| C. | Mg(OH)2+H2SO4═MgSO4+2H2O | D. | MgCl2$\frac{\underline{\;通电\;}}{熔融}$Mg+Cl2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将pH=4的某酸稀释10倍,测得其pH<5,则该酸为弱酸 | |
| B. | 0.1mol•L-1的NaHCO3溶液中C(Na+)=c(HCO3-)+c(H2CO3)+c(CO32-) | |
| C. | 0.1mol•L-1的NaHA溶液pH=5,则溶液:c(Na+)+c(H+)=c(OH-)+c(HA-)+c(A2-) | |
| D. | pH=4的醋酸与pH=10的氢氧化钠溶液等体积混合,所得溶液pH<7 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 溶液中的c(CO32-)增大 | B. | 溶液的pH减小 | ||
| C. | 溶液中的c(HCO3-)减小 | D. | 溶液中的c(OH-)增大 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com