
甲醛是一种重要的化工产品,可以利用甲醇脱氢制备,反应式如下:
①CH3OH(g) CH2O(g)+H2(g) ΔH1=+84.2 kJ·mol-1
CH2O(g)+H2(g) ΔH1=+84.2 kJ·mol-1
向反应体系中通入氧气,通过反应②2H2(g)+O2(g) 2H2O(g) ΔH2=-483.6 kJ·mol-1提供反应①所需热量,要使反应温度维持在700 ℃,则进料中甲醇与氧气的物质的量之比约为( )
2H2O(g) ΔH2=-483.6 kJ·mol-1提供反应①所需热量,要使反应温度维持在700 ℃,则进料中甲醇与氧气的物质的量之比约为( )
A.5.74∶1B.11.48∶1C.1∶1D.2∶1
 快乐小博士巩固与提高系列答案
快乐小博士巩固与提高系列答案科目:高中化学 来源:2014高考化学名师知识点精编 选修3物质结构与性质练习卷(解析版) 题型:选择题
在以下的分子或离子中,空间结构的几何形状不是三角锥形的是( )
A.NF3 B.CH3— C.BF3 D.H3O+
查看答案和解析>>
科目:高中化学 来源:2014高考化学名师知识点精编 专题7元素周期表与元素周期律练习卷(解析版) 题型:填空题
短周期的五种元素A、B、C、D、E,原子序数依次增大。A、B、C三种元素电子层数之和是5。A、B两元素原子最外层电子数之和等于C元素原子最外层电子数;B元素原子最外电子层上的电子数是它的电子层数的2倍,A与D可以形成原子个数比分别为1∶1和2∶1的两种液态化合物;E单质用于净化水质。
请回答:
(1)写出D在元素周期表中的位置 ,
E的原子结构示意图是 。
下列可以验证C与D两元素原子得电子能力强弱的实验事实是 (填写编号)。
A.比较这两种元素的气态氢化物的沸点
B.比较只有这两种元素所形成的化合物中的化合价
C.比较这两种元素的气态氢化物的稳定性
D.比较这两种元素的单质与氢气化合的难易
(2)由A、B两种元素组成的最简单的化合物,写出其电子式 。
(3)均由A、B、C、D四种元素组成的甲、乙两种化合物,都既可以与盐酸反应又可以与NaOH溶液反应,甲为无机盐,其化学式为 ,乙为天然高分子化合物的水解产物,且是同类物质中相对分子质量最小的,其结构简式为 。
(4)胶态磁流体在医学上有重要的用途,而纳米级Fe3O4是磁流体中的重要粒子,其制备过程可简单表示如下:
①将化合物CA3通入等物质的量的FeSO4、Fe2(SO4)3的混合溶液中,生成两种碱,写出该反应过程的总的离子方程式 。
②上述反应生成的两种碱继续作用,得到Fe3O4。
(5)已知下表数据:
物质 | Fe(OH)2 | Fe(OH)3 |
Ksp/25 ℃ | 2.0×10-16 | 4.0×10-36 |
若使混合液中FeSO4、Fe2(SO4)3的浓度均为2.0 mol·L-1,则混合液中c(OH-)不得大于 mol·L-1。
查看答案和解析>>
科目:高中化学 来源:2014高考化学名师知识点精编 专题6原子结构化学键练习卷(解析版) 题型:选择题
日本大地震引发的福岛第一核电站核泄漏事故,造成放射性物质碘和铯 向外界泄漏。下列相关说法错误的是( )
向外界泄漏。下列相关说法错误的是( )
A.每个 原子中有82个中子
原子中有82个中子
B.CsOH的碱性比KOH强
C.KIO3是碘的最高价氧化物的水化物的盐
D.I-比F-还原性强
查看答案和解析>>
科目:高中化学 来源:2014高考化学名师知识点精编 专题5化学能与热能练习卷(解析版) 题型:填空题
通常人们把拆开1 mol某化学键所吸收的能量看成该化学键的键能。键能的大小可以衡量化学键的强弱,也可以估算化学反应的反应热(ΔH),化学反应的ΔH等于反应中断裂旧化学键的键能之和与反应中形成新化学键的键能之和的差。
化学键 | Si—O | Si—Cl | H—H | H—Cl | Si—Si | Si—C |
键能/kJ·mol-1 | 460 | 360 | 436 | 431 | 176 | 347 |
请回答下列问题:
(1)比较下列两组物质的熔点高低(填“>”或“<”)。
SiC Si;SiCl4 SiO2。
(2)如图立方体中心的“”表示硅晶体中的一个原子,请在立方体的顶点用“”表示出与之紧邻的硅原子。

(3)工业上用高纯硅可通过下列反应制取:SiCl4(g)+2H2(g) Si(s)+4HCl(g),该反应的反应热ΔH= kJ/mol。
Si(s)+4HCl(g),该反应的反应热ΔH= kJ/mol。
查看答案和解析>>
科目:高中化学 来源:2014高考化学名师知识点精编 专题5化学能与热能练习卷(解析版) 题型:选择题
下列表述中正确的是( )
A.已知2H2(g)+O2(g) 2H2O(g) ΔH=-483.6 kJ/mol,则氢气的燃烧热为241.8 kJ
2H2O(g) ΔH=-483.6 kJ/mol,则氢气的燃烧热为241.8 kJ
B.由C(石墨,s) C(金刚石,s) ΔH=+11.9 kJ·mol-1可知,金刚石比石墨稳定
C(金刚石,s) ΔH=+11.9 kJ·mol-1可知,金刚石比石墨稳定
C.同温同压下,H2(g)+Cl2(g) 2HCl(g)在光照和点燃条件的ΔH不同
2HCl(g)在光照和点燃条件的ΔH不同
D.任何一个化学变化都伴随着能量的变化
查看答案和解析>>
科目:高中化学 来源:2014高考化学名师知识点精编 专题4氧化还原反应练习卷(解析版) 题型:选择题
下列有关说法正确的是( )
A.1 mol Cl2参加反应转移电子数一定为2NA
B.在反应KIO3+6HI KI+3I2+3H2O中,每生成3 mol I2转移的电子数为6NA
KI+3I2+3H2O中,每生成3 mol I2转移的电子数为6NA
C.根据反应中HNO3(稀)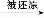 NO,而HNO3(浓)
NO,而HNO3(浓)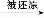 NO2可知,氧化性HNO3(稀)>HNO3(浓)
NO2可知,氧化性HNO3(稀)>HNO3(浓)
D.含有大量NO3—的溶液中,不能同时大量存在H+、Fe2+、Cl-
查看答案和解析>>
科目:高中化学 来源:2014高考化学名师知识点精编 专题3离子反应练习卷(解析版) 题型:选择题
下列离子方程式书写正确的是( )
A.显蓝色的淀粉溶液中通入足量SO2后变成无色溶液:I2+SO2+2H2O 2I-+SO42—+4H+
2I-+SO42—+4H+
B.已知电离平衡常数:H2CO3>HClO>HCO32—,向NaClO溶液中通入少量二氧化碳:2ClO-+CO2+H2O 2HClO+CO42—
2HClO+CO42—
C.NH4HCO3溶液与过量NaOH溶液反应:NH4++OH- NH3↑+H2O
NH3↑+H2O
D.FeI2溶液中通入过量Cl2:2Fe2++2I-+2Cl2 2Fe3++I2+4Cl-
2Fe3++I2+4Cl-
查看答案和解析>>
科目:高中化学 来源:2014高考化学名师知识点精编 专题21化学实验基础练习卷(解析版) 题型:选择题
下列装置不能完成的实验是( )
ABCD
装
置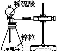
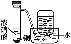

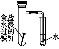
实
验结合秒表粗略测量锌与硫酸的反应速率制备并收集少量NO气体验证温度对化学平衡的影响铁的析氢腐蚀实验
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com