
【题目】将镁、铝的混合物共0.2mol,溶于200mL 4molL﹣1的盐酸溶液中,然后再滴加2molL﹣1的NaOH溶液.请回答下列问题:
(1)若在滴加NaOH溶液的过程中,沉淀质量m 随加入NaOH溶液的体积V变化情况如图所示.当V1=160mL时,则金属粉末中n (Al)=mol
(2)0~V1段发生的反应的离子方程式为;
(3)若在滴加NaOH溶液的过程中,欲使Mg2+、Al3+刚好沉淀完全,则滴入NaOH溶液的体积V(NaOH)=mL;
(4)若镁、铝的混合物仍为0.2mol,其中镁粉的物质的量分数为a,改用200mL 4molL﹣1的硫酸溶解此混合物后,再加入840mL 2molL﹣1的NaOH溶液,所得沉淀中无Al(OH)3 , 则a的取值范围为 .
【答案】
(1)0.08 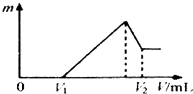
(2)H++OH﹣=H2O
(3)400
(4)0.6≤a<1
【解析】解:(1)当V1=160mL时,此时,溶液是MgCl2、AlCl3和NaCl的混合液, 由Na+离子守恒可知,n(NaCl)=n(Na+)=n(NaOH)=0.16L×2mol/L=0.32mol,
200mL 4molL﹣1的盐酸溶液中含有氯化氢的物质的量为:4mol/L×0.2L=0.8mol,
设混合物中含有MgCl2xmol、AlCl3为ymol,则:
根据Mg原子、Al原子守恒有:x+y=0.2,
根据Cl﹣离子守恒有:2x+3y=0.8﹣0.32=0.48,
联立方程解得:x=0.12、y=0.08,
所以金属粉末中:n(Mg)=0.12mol、n(Al)=y=0.08mol,
故答案为:0.08;(2)0~V1段,滴入氢氧化钠溶液后没有生成沉淀,说明盐酸过量,滴入的氢氧化钠与氯化氢反应生成氯化钠和水,反应的离子方程式为:H++OH﹣=H2O,
故答案为:H++OH﹣=H2O;(3)当溶液中Mg2+、Al3+恰好沉淀完全时,此时,溶液是NaCl溶液,根据Cl﹣离子和Na+离子守恒有:n(Na+)=n(NaCl)=(HCl)=4mol/L×0.2L=0.8mol,
所以需要加入氢氧化钠溶液体积为:V(NaOH)= ![]() =0.4L=400mL,
=0.4L=400mL,
故答案为:400;(4)由于为金属混合物,则a<1,Al的物质的量为:0.2(1﹣a)mol,反应后的混合溶液,再加入840mL 2molL﹣1的NaOH溶液,所得沉淀中无Al(OH)3 , 则溶质为硫酸钠、偏铝酸钠,根据铝元素守恒可知:n(NaAlO2)=0.2(1﹣a)mol,
根据钠离子守恒,应满足:n(NaOH)≥2n(Na2SO4)+n(NaAlO2),即0.84×2≥2×0.2×4+0.2(1﹣a),
解得:a≥0.6,
所以a的取值范围为:故0.6≤a<1,
故答案为:0.6≤a<1.
(1)根据图象可知,在滴加NaOH溶液到体积V1=160mL过程中,没有沉淀生成,说明盐酸有剩余,滴加的NaOH用于中和剩余盐酸,V1=160mL时,剩余的HCl与滴加的NaOH恰好完全反应,溶液是MgCl2、AlCl3和NaCl混合液,根据Mg原子、Al原子、Cl﹣离子、Na+离子守恒,列方程求算n(Al);(2)0~V1段滴入的氢氧化钠溶液与剩余的氯化氢反应生成氯化钠和水;(3)当溶液中Mg2+、Al3+恰好沉淀完全时,即沉淀达到最大值,此时,溶液是NaCl溶液,根据Cl﹣离子和Na+离子守恒有n(Na+)=n(NaCl)=(HCl)求出n(NaOH),再利用V= ![]() 计算滴入NaOH溶液的体积;(4)反应后的混合溶液,再加840mL 2molL﹣1的NaOH溶液,所得沉淀中无Al(OH)3 , 溶质为硫酸钠、偏铝酸钠,由于为金属混合物,则a<1,根据钠离子守恒,应满足n(NaOH)≥2n(Na2SO4)+n(NaAlO2),根据铝元素守恒用a表示出n(NaAlO2),据此确定a的取值范围.
计算滴入NaOH溶液的体积;(4)反应后的混合溶液,再加840mL 2molL﹣1的NaOH溶液,所得沉淀中无Al(OH)3 , 溶质为硫酸钠、偏铝酸钠,由于为金属混合物,则a<1,根据钠离子守恒,应满足n(NaOH)≥2n(Na2SO4)+n(NaAlO2),根据铝元素守恒用a表示出n(NaAlO2),据此确定a的取值范围.


科目:高中化学 来源: 题型:
【题目】浅绿色的Fe (NO3)2溶液中逐滴加入少量的稀硫酸时,溶液的颜色变化应该是
A. 颜色变浅 B. 变为血红色 C. 没有改变 D. 变为黄色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氧化还原反应在生产生活中有着重要的应用.请按要求写出相应的方程式.
(1)将含SO2的废气通入含Fe2+(催化剂)的溶液中,常温下可使SO2转化为SO24﹣ , 其总反应为2SO2+O2+2H2O=2H2SO4 . 上述总反应分两步进行,第一步反应的离子方程式为4Fe2++O2+4H+=4Fe3++2H2O,写出第二步反应的离子方程式: .
(2)pH=3.6时,碳酸钙与硫酸铝反应可制备碱式硫酸铝[Al2(SO4)x(OH)6﹣2x]溶液.若溶液的pH偏高,则碱式硫酸铝产率降低且有气泡产生,用化学方程式表示其原因: .
(3)ClO2是一种高效安全的杀菌消毒剂.氯化钠电解法生产ClO2工艺原理示意图如下: 
①写出氯化钠电解槽内发生反应的离子方程式: .
②写出ClO2发生器中的化学方程式,并标出电子转移的方向及数目: .
③ClO2能将电镀废水中的CN﹣离子氧化成两种无毒气体,自身被还原成Cl﹣ . 写出该反应的离子方程式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中错误的是( )
A.手性催化剂主要催化一种手性分子的合成
B.原子晶体的熔点一定比金属晶体的高
C.元素电负性越大的原子,吸引电子的能力越强
D.原子晶体中原子以共价键结合,具有键能大、熔点高、硬度大的特性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求填空:
(1)由乙烯制取聚乙烯的化学方程: .
(2)写出下列物质的结构简式; ①2,3﹣二甲基戊烷
②3﹣甲基﹣2﹣戊烯
③间二甲苯
(3)分子中含有5个碳原子的链状单炔烃的分子式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关SO2与SiO2的比较,正确的是
A.它们均为酸性氧化物
B.都溶于水,都能与强碱反应
C.S元素和Si元素化合价都为+4价,因此从氧化还原角度考虑他们具有一样的性质
D.SiO2可与HF反应,这是SiO2作为酸性氧化物的通性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关生活中化学的叙述中,正确的是
A.只用米汤就能检验出食盐中是否加碘
B.可用热的纯碱溶液清洗油污
C.“光化学烟雾”的形成与二氧化硫有关
D.用硅单质制光导纤维
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分析实验中出现下列现象对所配溶液的浓度有何影响:
(1)①浓硫酸溶解后未冷却至室温即转移至容量瓶中进行定容,(填“偏高”、“偏低”或“无影响”);
②定容时仰视刻度线,;填“偏高”、“偏低”或“无影响”);
③量取好浓硫酸倒入烧杯溶解后,用水洗涤量筒2~3次,将洗涤液倒入烧杯中, . (填“偏高”、“偏低”或“无影响”);
(2)7.8g镁铝合金与足量的稀盐酸反应,生成氢气的体积为8.96L(标准状况),则此反应中转移电子的数目为 , 镁和铝分别产生氢气的体积之比为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法错误的是( )
A.油脂在人体内通过酶的参与可水解为高级脂肪酸和甘油
B.油脂主要在小肠中消化吸收
C.磷脂对人体吸收维生素A E是有利的
D.同质量的脂肪在体内氧化时放出的能量比糖类和蛋白质高得多,故脂肪是人体提供能量的主要物质
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com