
 .
. .
.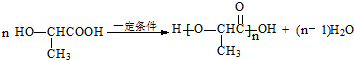 .
.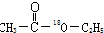 的合成路线,合成路线流程图示例如下:CH2-CH2$\stackrel{HBr}{→}$CH3CH2Br$→_{△}^{NaOH溶液}$CH3CH2OH.
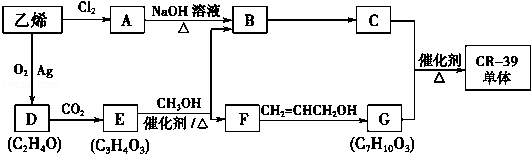
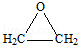
的合成路线,合成路线流程图示例如下:CH2-CH2$\stackrel{HBr}{→}$CH3CH2Br$→_{△}^{NaOH溶液}$CH3CH2OH. 分析 乙烯和氯气发生加成反应生成A,A的结构简式为:CH2ClCH2Cl,A和氢氧化钠的水溶液发生取代反应生成B,B的结构简式为:CH2OHCH2OH,乙烯被氧气氧化生成D,在D、E的分子中,都只有一种化学环境的氢原子,结合D的分子式知,D是 ,
,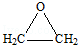 和二氧化碳反应生成E,E为五元环状化合物,所以E的结构简式为:
和二氧化碳反应生成E,E为五元环状化合物,所以E的结构简式为: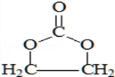 ,
,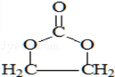 和甲醇反应生成乙二醇和F,则F的结构简式为:
和甲醇反应生成乙二醇和F,则F的结构简式为: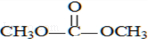 ,F和丙烯醇反应生成G,根据题给信息知,G的为
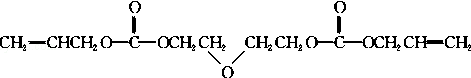
,F和丙烯醇反应生成G,根据题给信息知,G的为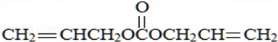 ,C是HOCH2CH2OCH2CH2OH,
,C是HOCH2CH2OCH2CH2OH,
(5)以CH2=CH2和H218O为原料,其他无机试剂任选合成 ,先制备乙酸:CH2=CH2催化氧化生成CH3CHO、CH3CHO催化氧化生成CH3COOH,然后用乙烯和H18O-H发生加成反应制备C2H5-18OH,最后CH3COOH、C2H5-18OH发生酯化反应生成CH3CO18OC2H5,据此分析解答.
,先制备乙酸:CH2=CH2催化氧化生成CH3CHO、CH3CHO催化氧化生成CH3COOH,然后用乙烯和H18O-H发生加成反应制备C2H5-18OH,最后CH3COOH、C2H5-18OH发生酯化反应生成CH3CO18OC2H5,据此分析解答.
解答 解:乙烯和氯气发生加成反应生成A,A的结构简式为:CH2ClCH2Cl,A和氢氧化钠的水溶液发生取代反应生成B,B的结构简式为:CH2OHCH2OH,乙烯被氧气氧化生成D,在D、E的分子中,都只有一种化学环境的氢原子,结合D的分子式知,D是 ,
, 和二氧化碳反应生成E,E为五元环状化合物,所以E的结构简式为:
和二氧化碳反应生成E,E为五元环状化合物,所以E的结构简式为: ,
, 和甲醇反应生成乙二醇和F,则F的结构简式为:
和甲醇反应生成乙二醇和F,则F的结构简式为: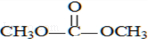 ,F和丙烯醇反应生成G,根据题给信息知,G的为
,F和丙烯醇反应生成G,根据题给信息知,G的为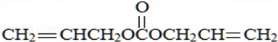 ,C是HOCH2CH2OCH2CH2OH,
,C是HOCH2CH2OCH2CH2OH,
(1)C是HOCH2CH2OCH2CH2OH,C中含有醇羟基和醚基,
a、C中含有醇羟基,所以能与乙酸发生酯化反应,故a正确;
b、C中不含羧基,所以不能与乙醇发生酯化反应,故b错误;
c、1个C分子中含有两个醇羟基,所以1mol C最多能与2mol Na反应,故c正确;
d、根据C的分子式可知,C为饱和结构,不可能含有醛基,所以C的同分异构体不能发生银镜反应,故d正确;
故答案为:acd;
(2)乙烯和氯气发生加成反应生成A;B是乙二醇,所以B中官能团是羟基,故答案为:加成反应;羟基;
(3)①通过以上分析知,D的结构简式为: ,故答案为:
,故答案为: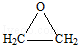 ;
;
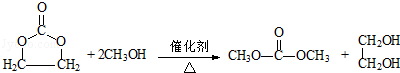
②在催化剂、加热条件下,E和甲醇发生取代反应,反应方程式为: ,
,
故答案为: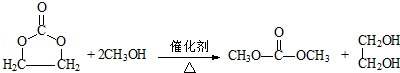 ;
;
(4)F的结构简式为: ,F的一种同分异构体K,其分子中不同化学环境的氢原子个数比是3:1:1:1,且能与NaHCO3反应,说明含有羧基,则K的结构简式为:
,F的一种同分异构体K,其分子中不同化学环境的氢原子个数比是3:1:1:1,且能与NaHCO3反应,说明含有羧基,则K的结构简式为: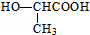 ,在一定条件下,2-羟基丙酸发生缩聚反应,反应方程式为
,在一定条件下,2-羟基丙酸发生缩聚反应,反应方程式为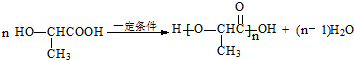 ,
,
故答案为: ;
;
(5)以CH2=CH2和H218O为原料,其他无机试剂任选合成 ,先制备乙酸:CH2=CH2催化氧化生成CH3CHO、CH3CHO催化氧化生成CH3COOH,然后用乙烯和H18O-H发生加成反应制备C2H5-18OH,最后CH3COOH、C2H5-18OH发生酯化反应生成CH3CO18OC2H5,所以合成流程图为CH2=CH2$→_{△}^{催化剂、O_{2}}$CH3CHO$→_{△}^{催化剂、O_{2}}$CH3COOH、CH2=CH2+H18O-H$\stackrel{H_{2}SO_{4}/△、加压}{→}$C2H518OH$→_{浓硫酸、△}^{CH_{3}COOH}$CH3CO18OC2H5,
,先制备乙酸:CH2=CH2催化氧化生成CH3CHO、CH3CHO催化氧化生成CH3COOH,然后用乙烯和H18O-H发生加成反应制备C2H5-18OH,最后CH3COOH、C2H5-18OH发生酯化反应生成CH3CO18OC2H5,所以合成流程图为CH2=CH2$→_{△}^{催化剂、O_{2}}$CH3CHO$→_{△}^{催化剂、O_{2}}$CH3COOH、CH2=CH2+H18O-H$\stackrel{H_{2}SO_{4}/△、加压}{→}$C2H518OH$→_{浓硫酸、△}^{CH_{3}COOH}$CH3CO18OC2H5,
故答案为:CH2=CH2$→_{△}^{催化剂、O_{2}}$CH3CHO$→_{△}^{催化剂、O_{2}}$CH3COOH、CH2=CH2+H18O-H$\stackrel{H_{2}SO_{4}/△、加压}{→}$C2H518OH$→_{浓硫酸、△}^{CH_{3}COOH}$CH3CO18OC2H5.
点评 本题考查有机物推断和合成,为高频考点,侧重考查学生分析推断及合成设计能力,把握有机物官能团及其性质关系、物质之间的转化是解本题关键,难点是合成路线设计,可以根据反应物设计路线形成生成物,也可以根据生成物采用逆向思维方法合成路线设计,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 在0℃、101kPa条件下,11.2L丁烷中含极性共价键数目为5NA | |
| B. | 含23g钠元素的Na2O和Na2O2混合物中阴离子数目介于0.5NA和NA之间 | |
| C. | 5NH4NO3$\frac{\underline{\;\;△\;\;}}{\;}$4N2↑+2HNO3+9H2O中氧化产物比还原产物每多14g,转移电子数为15NA | |
| D. | 用惰性电极电解饱和碳酸钠溶液时,电路上通过2mol电子时产生气体分子总数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 68g KHSO4晶体中含有SO42-的数目为0.5NA | |
| B. | 把含0.1molFeCl3的浓溶液加入沸水中形成0.1NA个氢氧化铁胶粒 | |
| C. | 标况下2.24L丙烯分子中含有的共用电子对数目为0.9NA | |
| D. | 把5mL 11.2mol/L的浓盐酸与足量的MnO2固体混合,加热充分反应后,把产生的气体完全溶于水时,转移电子的数目为0.014NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用无水硫酸铜可检验酒精中是否有水 | |
| B. | 加生石灰进行过滤,可除去酒精中的水 | |
| C. | 用酒精可萃取出碘水中的碘 | |
| D. | 医院用100%酒精进行杀菌消毒 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碳酸钠(固体) | B. | 水 | C. | 稀盐酸 | D. | 硫酸铵(固体) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
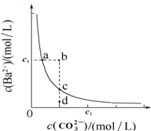
| A. | 通过蒸发可以使溶液由d点变到c点 | |
| B. | b点有BaCO3沉淀生成 | |
| C. | 升高温度,可以使d点变为c点 | |
| D. | 在a点加入Na2CO3,达平衡时c(Ba2+)≠c(CO32-),其Ksp大于c点对应的Ksp |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 32gO2所含有的原子数目为NA | |
| B. | 0.5mol CO2含有的原子数目为1.5 NA | |
| C. | 1mol H2O含有的水分子数目为NA | |
| D. | 0.5NA个氧气分子的物质的量是0.5 mol |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com