
下列各组离子,在指定的环境中一定能大量共存的是( )
A.常温下,在c(H+)/c(OH-)=1×1012的溶液中:I-、Cl-、NO3-、Na+
B.在能使石蕊变红色的溶液中:Na+、S2-、SO42-、CO32-
C.在加入铝粉能产生H2的溶液中:NH4+、Na+、NO3-、Cl-
D.常温下由水电离出的c(H+)=1×10-12mol·L-1的溶液中:K+、Cl-、NO3-、Na+
科目:高中化学 来源:2016-2017学年青海省高一上月考一化学试卷(解析版) 题型:选择题
某同学按下列步骤配制500 mL 0.20 mol·L-1NAOH溶液,请回答有关问题。
实验步骤 | 有关问题 |
(1)计算所需NAOH的质量 | 需要NAOH的质量为 g |
(2)称量NAOH固体 | 称量过程中主要用到的仪器是 |
(3)将NAOH加入100 mL烧杯中,加适量蒸馏水溶解 | 为加快溶解,可采取的措施是 |
(4)将烧杯中的溶液转移至500 mL容量瓶中 | 为防止溶液溅出,应该采取的措施是 |
(5)向容量瓶中加蒸馏水至刻度线 | 在进行此操作时应注意的问题是 |
查看答案和解析>>
科目:高中化学 来源:2016-2017学年内蒙古高一上月考一化学卷(解析版) 题型:选择题
在相同条件下,两种物质的量相同的气体必然 ( )
A.体积均为22.4L B .具有相同的体积
.具有相同的体积
C.是双原子分子 D.具有相同的原子数目
查看答案和解析>>
科目:高中化学 来源:2017届福建省龙岩市五校高三上学期期中化学试卷(解析版) 题型:推断题
常见无机物A、B、C、D存在如图转化关系:
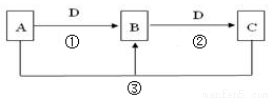
(1)若D是氯碱工业的主要产品,B有两性氢氧化物,则反应 ②的离子方程式是: 。
②的离子方程式是: 。
(2)若A是一种碱性气体,常用作制冷剂,B是汽车尾气之一,遇空气会变色,则反应①的化学方程式为 。
(3)若A为常见挥发性强酸,D是生产生活中用量最大用途最广的金属单质,,则B的化学式可能是 ,写出反应②的离子方程式为 。
(4)若A、C、D都是常见气体,C是形成酸雨的主要气体,则反应③的化学方程式 。
(5)若A、B、C的水溶液均显碱性,焰色反应均为黄色,D为CO2,用离子方程式解释B溶液显碱性的原因(用离子方程式表示)___________,举出C的一种用途_______。
查看答案和解析>>
科目:高中化学 来源:2017届福建省龙岩市五校高三上学期期中化学试卷(解析版) 题型:选择题
向KOH溶液中通入8.96 L(标准状况)氯气恰好完全反应生成三种含氯盐: 0.6molKCl、0.1molKClO和X。则X是( )
A.0.1molKClO4 B.0.1molKClO3 C.0.1molKClO2 D.0.2molKClO
查看答案和解析>>
科目:高中化学 来源:2017届北京市高三上学期期中化学试卷(解析版) 题型:简答题
“C1化学”是指以碳单质或分子中含1个碳原子的物质(如CO、CO2、CH4、CH3OH等)为原料合成工业产品的化学工艺,对开发新能源和控制环境污染有重要意义。
(1)一定温度下,在两个容积均为2 L的密闭容器中,分别发生反应:
CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H=﹣49.0kJ/mol。相关数据如下:
CH3OH(g)+H2O(g) △H=﹣49.0kJ/mol。相关数据如下:
容器 | 甲 | 乙 |
反应物投入量 | 1 mol CO2(g)和3 mol H2(g) | 1 mol CH3OH(g)和1 mol H2O(g) |
平衡时c(CH3OH) | c1 | c2 |
平衡时能量变化 | 放出29.4 kJ | 吸收a kJ |
请回答:
①c1 c2(填“>”、“<”或“=”);a = 。
②若甲中反应10 s时达到平衡,则用CO2来表示甲中反应从开始到平衡过程中的平均反应速率是 mol/(L·s)。
(2)压强为p1时 ,向体积为1 L的密闭容器中充入b mol CO和2b mol H2,发生反应CO(g)+2H2(g) CH3OH(g)。平衡时CO的转化率与温度、压强的关系如图所示。请回答:
CH3OH(g)。平衡时CO的转化率与温度、压强的关系如图所示。请回答:
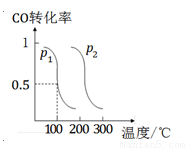
①该反应属于 (填“吸”或“放”)热反应;p1 p2(填“>”、“<”或“=”)。
②100℃时,该反应的平衡常数K= (用含b的代数式表示)。
(3)治理汽车尾气的反应是2NO(g)+2CO(g)?2CO2(g)+N2(g) △H<0。在恒温恒容的密闭容器中通入n(NO):n(CO)=1:2的混合气体,发生上述反应。下列图像正确且能说明反应在进行到t1时刻一定达到平衡状态的是 (选填字母)。




a b c d
查看答案和解析>>
科目:高中化学 来源:2017届北京市高三上学期期中化学试卷(解析版) 题型:选择题
为研究沉淀的生成及其转化,某小组进行如下实验。关于该实验的分析不正确的是
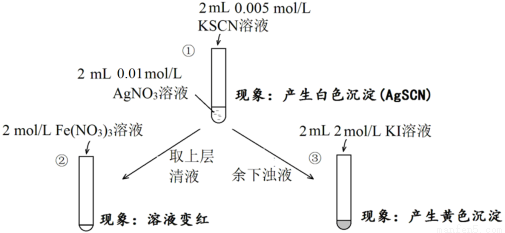
A.①浊液中存在平衡:AgSCN(s) Ag+(aq)+SCN-(aq)
Ag+(aq)+SCN-(aq)
B.②中颜色变化说明上层清液中含有SCN-
C.③中颜色变化说明有AgI生成
D.该实验可以证明AgI比AgSCN更难溶
查看答案和解析>>
科目:高中化学 来源:2016-2017学年浙江省杭州市高一10月月考化学卷(解析版) 题型:填空题
(1)有以下几种物质:①食盐晶体 ②铜 ③KNO3溶液 ④熔融的氢氧化钾 ⑤液态氯化氢 ⑦干冰 ⑧酒精。回答以下问题(填序号):
(1)物质中构成的微粒只能在固定位置上振动的是 ;
(2)以上物质中能导电且属于电解质的是 ;
(3)以上物质中属于非电解质的是 ;
(4)在标准状况下,由CO和CO2组成的混合气体为6.72 L,质量为12 g,此混合物中CO和CO2物质的量之比是________________,CO2的体积分数是________________。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年四川省高二10月月考化学卷(解析版) 题型:选择题
COCl2(g) CO(g)+Cl2(g) ΔH>0,当反应达到平衡时,下列措施:①升温 ②恒容通入惰性气体 ③增加CO浓度 ④减压 ⑤加催化剂 ⑥恒压通入惰性气体,能提高COCl2转化率的是
CO(g)+Cl2(g) ΔH>0,当反应达到平衡时,下列措施:①升温 ②恒容通入惰性气体 ③增加CO浓度 ④减压 ⑤加催化剂 ⑥恒压通入惰性气体,能提高COCl2转化率的是
A.①②④ B.①④⑥ C.②③⑤ D.③⑤⑥
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com