
分析 Ⅰ.(1)依据燃烧热概念是1mol可燃物完全燃烧生成稳定氧化物放出的热量,根据题干所给量结合热化学方程式书写方法,标注物质聚集状态和对应焓变;
(2)由盖斯定律可知,①CH3OH(g)+H2O(g)=CO2(g)+3H2(g)△H1=+49.0kJ•mol-1、③H2(g)+$\frac{1}{2}$O2(g)═H2O(g)△H=-241.8kJ•mol-1,①+③得到反应②;
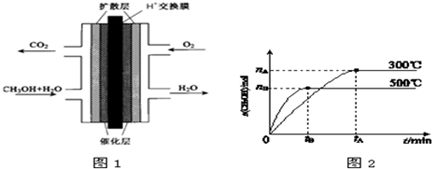
(3)甲醇燃料电池中,甲醇为负极,失电子发生氧化反应,电极反应结合电荷守恒和原子守恒写出为:CH3OH+H2O-6e-═6H++CO2,氧气在正极发生还原反应,电极反应式为:O2+4H++4e-═2H2O;
Ⅱ.(1)平衡常数是衡量反应进行程度的物理量,根据升高温度乙醇的物质的量减小,平衡逆向移动,判断平衡常数的变化;
(2)结合图象中甲醇物质的量变化计算用甲醇表示的反应速率,化学反应速率之比等于化学方程式计量数之比,以此计算H2的浓度变化表示的化学反应速率,根据化学反应速率是υ(H2)=2υ(CH3OH)计算得到;
(3)达到平衡时,正逆反应速率相等,混合气体的平均相对分子质量不再改变,CO、H2、CH3OH的浓度不再改变;
(4)将容器的容积压缩到原来的$\frac{1}{2}$,压强增大,反应速率增大,平衡向正反应方向移动,以此判断.
解答 解:Ⅰ.(1)在25℃、101kPa下,1mol CH3OH液体完全燃烧生成CO2和液态水时放出热量726.51kJ,则表示甲醇燃烧热的热化学方程式为:CH3OH(l)+$\frac{3}{2}$O2(g)=CO2(g)+2H2O(l)△H=-725.76kJ•mol-1,
故答案为:CH3OH(l)+$\frac{3}{2}$O2(g)=CO2(g)+2H2O(l)△H=-725.76kJ•mol-1;
(2)①CH3OH(g)+H2O(g)=CO2(g)+3H2(g)△H1=+49.0kJ•mol-1,
②CH3OH(g)+$\frac{1}{2}$O2(g)═CO2(g)+2H2(g)△H2,
③H2(g)+$\frac{1}{2}$O2(g)═H2O(g)△H=-241.8kJ•mol-1,
依据盖斯定律计算①+③得到反应②,则△H2=+49.0kJ•mol-1+(-241.8kJ•mol-1)=-192.8kJ•mol-1,
故答案为:-192.8kJ•mol-1;
(3)甲醇燃料电池中,甲醇中C元素的化合价升高,则甲醇为负极,失电子发生氧化反应,在酸性溶液中生成二氧化碳,电极反应结合电荷守恒和原子守恒写出为:CH3OH+H2O-6e-═6H++CO2,故答案为:CH3OH+H2O-6e-═6H++CO2;
Ⅱ.(1)由图象2可知升高温度乙醇的物质的量减少,平衡向逆反应方向移动,K减小,
故答案为:减小;
(2)500℃时,从反应开始到达到化学平衡,结合图象中甲醇物质的量变化计算用甲醇表示的反应速率,化学反应速率之比等于化学方程式计量数之比,以此计算H2的浓度变化表示的化学反应速率,υ(CH3OH)=$\frac{{n}_{B}}{{n}_{t}×3L}$mol/(L.min),故υ(H2)=2υ(CH3OH)=$\frac{2{n}_{B}}{3{t}_{B}}$mol/(L.min),
故答案为:$\frac{2{n}_{B}}{3{t}_{B}}$mol/(L.min);
(3)CO(g)+2H2(g)?CH3OH(g),达到平衡时,正逆反应速率相等,混合气体的平均相对分子质量不再改变,CO、H2、CH3OH的浓度不再改变,在体积不变时,气体的密度不变,不能作为判断是否达到平衡状态的依据,
a.CO、H2、CH3OH的浓度均不再变化是平衡的标志,故a正确;
b.反应前后气体质量不变,容器体积不变,反应过程中和平衡状态下混合气体的密度始终不改变,不能说明费用达到平衡状态,故b错误;
c.反应前后气体质量不变,气体物质的量变化,当混合气体的平均相对分子质量不再改变,说明反应达到平衡状态,故c正确;
d.化学反应速率之比等于化学方程式计算数之比,为正反应速率之比,v生成(CH3OH)=v消耗(CO)只能说明平衡正向进行时甲醇和一氧化碳的反应速率相同,不能说明反应达到平衡状态,当v生成(CH3OH)=v生成(CO)能说明反应达到平衡状态,故d错误;
e.混合气中n(CO):n(H2):n(CH3OH)=1:2:1,不能说明反应正逆反应速率相同,不能说明反应达到平衡状态,故e错误;
故答案为:ac;
(4)a.将容器的容积压缩到原来的 $\frac{1}{2}$,压强增大,正逆反应速率都增大,平衡向正反应方向移动,CH3OH的物质的量增加,氢气的物质的量减少,但体积改变影响大于平衡移动的影响,所以氢气浓度增大,故a错误;
b.缩小体积增大压强,正逆反应速率都增大,故b错误;
c.平衡向正反应方向移动,甲醇的物质的量增多,故c正确;
d.平衡向正反应方向移动,甲醇浓度增大,氢气浓度减小,故有$\frac{c({H}_{2})}{c(C{H}_{3}OH)}$减小,故d正确;
故答案为:cd.
点评 本题考查化学平衡的影响因素和化学平衡的标志,热化学方程式书写,原电池原理的理解应用等问题,题目难度中等,注意外界条件对化学平衡移动的影响以及平衡状态的判断角度.


科目:高中化学 来源: 题型:选择题
| A. | 35.6% | B. | 27% | C. | 10% | D. | 73% |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
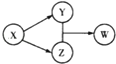 X、Y、Z、W四种物质的转化关系.下列组合中不符合该关系的是( )
X、Y、Z、W四种物质的转化关系.下列组合中不符合该关系的是( )| A | B | C | D | |
| X | HCl | Na2CO3 | Na2O2 | SO2 |
| Y | FeCl2 | CO2 | NaOH | Na2SO3 |
| Z | Cl2 | CaCO3 | Na2CO3 | H2SO4 |
| W | FeCl3 | Ca(HCO3)2 | NaHCO3 | NaHSO3 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
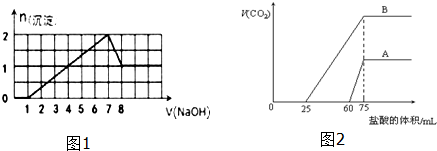
 向100mL 3mol/L的NaOH溶液中缓慢通入一定量的CO2,充分反应,测得最后溶液的PH>7.
向100mL 3mol/L的NaOH溶液中缓慢通入一定量的CO2,充分反应,测得最后溶液的PH>7.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 ,B
,B ,C
,C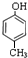 .
.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
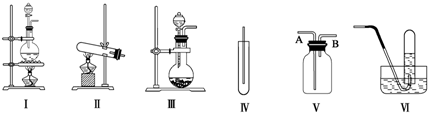
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
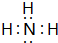 .实验室制取该种物质的化学方程式为Ca(OH)2+2NH4Cl$\frac{\underline{\;\;△\;\;}}{\;}$ 2NH3↑+CaCl2+2H2O.
.实验室制取该种物质的化学方程式为Ca(OH)2+2NH4Cl$\frac{\underline{\;\;△\;\;}}{\;}$ 2NH3↑+CaCl2+2H2O.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C3H8 | B. | C8H16 | C. | C8H8 | D. | C3H4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com