
| A. | 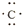 | B. | 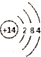 | C. | 1s22s2p4 | D. | 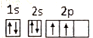 |
 53随堂测系列答案
53随堂测系列答案科目:高中化学 来源: 题型:解答题


查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 减少机动车尾气的排放,可以降低雾霾的发生 | |
| B. | 垃圾焚烧法已成为许多城市垃圾处理的主要方法之一,利用垃圾焚烧产生的热能发电或供热,能较充分地利用生活垃圾中的生物质能 | |
| C. | 推广使用煤液化技术,可减少二氧化碳等温室气体的排放 | |
| D. | 燃料电池是一种高效、环境友好的发电装置 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1 mol SO2 (g)的能量总和大于1 mo S(s)和1 mol O2(g)的能量总和 | |
| B. | 加入合适的催化剂,可增加单位质量的硫燃烧放出的热量 | |
| C. | S(g)+O2(g)→SO2(g)+Q1 kJ;Q1的值大于297.23 | |
| D. | 足量的硫粉与标况下1升氧气反应生成1升二氧化硫气体时放出297.23 kJ热量 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题



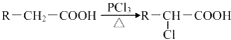

查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 只闭合K2,该装置将电能转化为化学能 | |
| B. | 只闭合K1,石墨棒周围溶液pH逐渐升高 | |
| C. | 只闭合K2,铁棒不会被腐蚀,属于牺牲阳极的阴极保护法 | |
| D. | 铁腐蚀的速度由大到小的顺序是:只闭合K1>都断开>只闭合K2 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 通入1molCl2:2Fe2++2Br-+2Cl2→4Cl-+Br2+2Fe3+ | |
| B. | 通入足量Cl2:2Fe2++4Br-+3Cl2→2Fe3++2Br2+6Cl- | |
| C. | 加入含2molBa(OH)2的溶液:Al3++SO42-+Ba2++4OH-→BaSO4↓+AlO2-+2H2O | |
| D. | 加入足量Ba(OH)2的溶液:Fe2++Al3++SO42-+Ba2++6OH-→Fe(OH)2↓+AlO2-+BaSO4↓+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题



 ;
; ;
;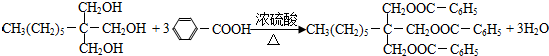 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验步骤 | 实验现象 |
| 1.将镁条用砂纸打磨后,放入沸水中;再向溶液中滴加酚酞溶液 | A.浮在水面上,熔成小球,做不定向运动,随之消失,溶液变成红色. |
| 2.向新制得的Na2S溶液中滴加少量新制的氯水 | B.有气体产生,溶液变成浅红色 |
| 3.将一小块钠放入滴有酚酞溶液的冷水中 | C.剧烈反应,迅速产生大量无色气体. |
| 4.将镁条投入稀盐酸中 | D.反应不十分剧烈,产生无色气体 |
| 5.将铝条投入稀盐酸中 | E.生成淡黄色沉淀 |
| 实验内容 | 实验现象 | 离子方程式 |
| 1 | ||
| 2 | ||
| 3 | ||
| 4 | ||
| 5 |
| 实验 序号 | 氯化镁固体中氯元素含量/% | 温度/℃ | 粉碎方式/ | 催化效果/g•g-1 |
| 1 | 70.97 | 20 | 滚动球磨 | 3.9×104 |
| 2 | 74.45 | 20 | 滚动球磨 | 5.0×104 |
| 3 | 74.45 | 20 | 振动球磨 | 5.9×104 |
| 4 | ω | 100 | 振动球磨 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com