
| A、1:1:1 |
| B、2:1:1 |
| C、3:2:3 |
| D、5:3:4 |
| 7 |
| 2 |
| 5 |
| 2 |
| 9 |
| 2 |
| 7 |
| 2 |
| 5 |
| 2 |
| 9 |
| 2 |


科目:高中化学 来源: 题型:
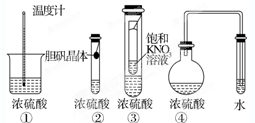 在实验探究课上,同学们积极思考,共设计出如图所示的四种实验方案用以验证浓硫酸的吸水性,其中在理论上可行的是( )
在实验探究课上,同学们积极思考,共设计出如图所示的四种实验方案用以验证浓硫酸的吸水性,其中在理论上可行的是( )| A、①②③④ | B、①③④ |
| C、①②④ | D、②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、高温时Na2O+SiO2=Na2SiO3 |
| B、高温时Na2CO3+SiO2=Na2SiO3+CO2↑ |
| C、高温时CaCO3+SiO2=CaSiO3+CO2↑ |
| D、高温时Na2CO3+6SiO2+CaCO3=Na2O+CaO+6SiO2+2CO2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、浓硝酸和稀硝酸都具有强氧化性 |
| B、铜和稀硝酸的反应属于置换反应 |
| C、在铜与浓硝酸的反应中,硝酸只体现氧化性,没有体现酸性 |
| D、可用铝或铁制容器盛装稀硝酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、温度计 | B、蒸馏烧瓶 |
| C、冷凝管 | D、烧杯 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①③ | B、②④ | C、②③ | D、①④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、该AgI胶粒带正电荷 |
| B、该AgI胶粒电泳时向阳极移动 |
| C、该AgI胶粒带负电荷 |
| D、该AgI胶粒不带电荷 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Cu2+、Ba2+、NO3-、Cl- |
| B、Mg2+、Na+、CO32-、SO42- |
| C、Ba2+、Mg2+、NO3-、Cl- |
| D、Fe3+、Ba2+、NO3-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com