
| A. |  H2 | B. |  浓盐酸 | C. |  浓硫酸 | D. |  CO2 |
科目:高中化学 来源: 题型:选择题
| A. | 有2个A原子 | B. | 有2个氧原子 | C. | 有1个A原子 | D. | 有1个氧原子 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 已知A、B、C、D和E都是元素周期表中前36号元素,它们的原子序数依次增大.A与其他4种元素既不在同一周期又不在同一主族.B和C属同一主族,D和E属同一周期,又知E是周期表中1~18列中的第7列元素.D的价电子数为2,D跟B可形成离子化合物,其晶胞结构如图.请回答:
已知A、B、C、D和E都是元素周期表中前36号元素,它们的原子序数依次增大.A与其他4种元素既不在同一周期又不在同一主族.B和C属同一主族,D和E属同一周期,又知E是周期表中1~18列中的第7列元素.D的价电子数为2,D跟B可形成离子化合物,其晶胞结构如图.请回答:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 微粒半径:O2-<F-<Na+<Li+ | |
| B. | 第一电离能:C<N<O | |
| C. | 元素的电负性:O>S>N>P | |
| D. | 热稳定性大小:SiH4<PH3<NH3<H2O<HF |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 如图装置是中学化学实验中常见的仪器,它除用于洗气外,还有其他用途:
如图装置是中学化学实验中常见的仪器,它除用于洗气外,还有其他用途:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
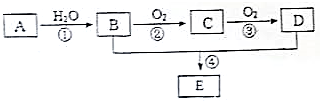 已知A的产量通常用来衡量一个国家的石油化工水平,现以A为主要原料合成一种物质E,其合成路线如图所示.
已知A的产量通常用来衡量一个国家的石油化工水平,现以A为主要原料合成一种物质E,其合成路线如图所示. .B、D分子中的官能团名称分别是羟基、羧基.
.B、D分子中的官能团名称分别是羟基、羧基.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
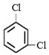
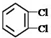 ;③35Cl、37Cl;
;③35Cl、37Cl;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | [Cu(H2O)4]SO4•H2O | B. | [Ag(NH3)2]OH | C. | KAl(SO4)2•12H2O | D. | Fe(SCN)3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 第VIA族的氧、硫、硒(Se)、碲(Te)等元素在化合物中常表现出多种价态,含第VIA族元素的化合物在研究和生产中有许多重要用途.请回答下列问题:
第VIA族的氧、硫、硒(Se)、碲(Te)等元素在化合物中常表现出多种价态,含第VIA族元素的化合物在研究和生产中有许多重要用途.请回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com