
1 1 |
2 1 |
 和
和 ;⑤
;⑤ 和
和
1 1 |
2 1 |


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 b.
b. c.
c.
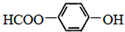 b.
b. c.
c.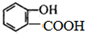
 的名称为
的名称为 核磁共振氢谱有
核磁共振氢谱有 .
.查看答案和解析>>
科目:高中化学 来源: 题型:
 一化学研究性学习小组对某工厂生产印刷电路板后所得废液进行探究(生产原理:2Fe3++Cu═2Fe2++Cu2+).请按要求完成下列探究报告.
一化学研究性学习小组对某工厂生产印刷电路板后所得废液进行探究(生产原理:2Fe3++Cu═2Fe2++Cu2+).请按要求完成下列探究报告.查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 温度 | 250℃ | 300℃ | 350℃ |
| K | 2.041 | 0.270 | 0.012 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、纯碱、烧碱均属于碱类 |
| B、CO2、SiO2、SO2均属于酸性氧化物 |
| C、醋酸、硫酸、硝酸均属于酸类 |
| D、Na2CO3、Na2SO3、NaCl均属于钠盐 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Na+、Ba2+、SO42-、Cl- |
| B、H+、Ag+、Cl-、NO3- |
| C、K+、H+、CO32-、Cl- |
| D、Cu2+、Fe3+、Cl-、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、电子数与质子数均为8 |
| B、中子数与质子数之差为10 |
| C、核电荷数与原子序数均为8 |
| D、中子数与质子数之和为18 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com