
分析 (1)由反应可知,A为二氧化硫,为酸性氧化物,根据硫酸的作用来回答;
(2)化合价降低的元素被还原;化合价升高后得到的产物为氧化产物;
(3)若反应消耗了3.2g Cu,物质的量为:0.05mol,则转移电子数0.05mol×2×6.02×1023,被还原的硫酸物质的量为0.05mol;
(4)将(2)中反应后所得到的溶液稀释后与足量BaCl2溶液反应,钡离子与硫酸根离子反应生成硫酸钡.
解答 解:(1)反应Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+A↑+2H2O中,A物质可以导致酸雨的形成,则A是二氧化硫,应该属于酸性氧化物,在参加反应的硫酸中,被还原的硫酸是1mol与未被还原的硫酸是1mol,其物质的量之比为1:1,
故答案为:d;
(2)化合价降低的元素被还原,所以被还原的元素是硫;化合价升高后得到的产物为氧化产物,即氧化产物为:CuSO4,故答案为:硫;CuSO4;
(3)若反应消耗了3.2g Cu,物质的量为:0.05mol,则转移电子数0.05mol×2×6.02×1023,被还原的硫酸物质的量为0.05mol;故答案为:6.02×1022;0.05;
(4)将(2)中反应后所得到的溶液稀释后与足量BaCl2溶液反应,钡离子与硫酸根离子反应生成硫酸钡,离子方程式为:Ba2++SO42-=BaSO4↓,故答案为:Ba2++SO42-=BaSO4↓.
点评 本题考查较为综合,涉及氧化还原反应、浓硫酸、二氧化硫的性质以及离子方程式的书写,侧重于学生的分析能力和计算能力的考查,为高考常见题型,难度中等,注意把握反应的相关方程式,结合方程式计算.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:多选题
| 难溶电解质 | AgCl | AgBr | AgI | Ag2SO4 | Ag2CrO4 |
| Ksp | 1.8×10-10 | 5.4×10-13 | 8.5×10-17 | 1.4×10-5 | 1.12×10-12 |
| A. | 由溶度积常数不能判断相应物质的溶解性大小 | |
| B. | 将等体积的4×10-3 mol/L的AgNO3溶液和4×10-3mol/L K2CrO4溶液混合,有Ag2CrO4沉淀产生 | |
| C. | 向AgCl的悬浊液中滴加饱和NaBr溶液不能得到黄色AgBr | |
| D. | 向100 mL 0.02mol/L的NaSO4溶液中加入100mL0.02mol/L的AgNO3溶液,有白色沉淀生成 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将容器体积变为原来一半 | B. | 压强变为原来一半 | ||
| C. | 加入2n molCO,2n molH2O | D. | 加入2n molCO2和2n molH2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
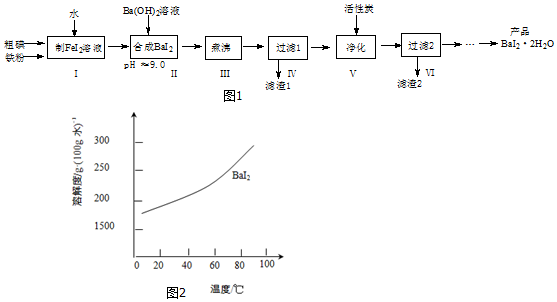
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
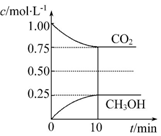
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | a=4 | |
| B. | S2O32-是还原剂 | |
| C. | 将Y均匀分散到水中形成的体系具有丁达尔效应 | |
| D. | 每有3 mol Fe2+参加反应,反应中转移的电子总数为5 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2mol•L-1 | B. | 3 mol•L-1 | C. | 1mol•L-1 | D. | 0.5 mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com