
���� ��1����������������������ɵ��������������ʵ����������÷�Ӧ���ʹ�ʽ��������������ƽ����Ӧ���ʣ�
��2�������2min�������ӵ����ʵ����ı仯�����ٸ���ƽ����Ӧ���ʹ�ʽ���㣻
��3������Ũ���뷴Ӧ���ʵĹ�ϵ������
��� �⣺��1����Ӧǰ�������������ʵ���Ϊ0��
Fe+H2SO4=FeSO4 +H2 ��
56g 1mol 22.4L
2.8g 0.05mol 1.12L
v��FeSO4 ��=$\frac{��c}{��t}$=$\frac{\frac{0.05mol}{0.1L}}{2min}$0.25 mol/��L��min����
����ǰ2min����FeSO4��ʾ��ƽ����Ӧ������ 0.25 mol/��L��min����
��2����Ӧǰ��������ʵ���Ϊ=100mL��2mol•L-1=0.02mol���������ʵ���Ϊ$\frac{8.4g}{56g/mol}$=0.15mol����Ϸ���ʽ֪����������ͨ����1��֪��ǰ�����ӣ�����Ӧ2.8g����ʣ5.6g����4minʱ������Ӧ5.6g��
Fe+H2SO4=FeSO4 +H2 ��
56g 1 mol
5.6g 0.1mol
������������ʵ����ı仯��Ϊ0.1mol��
���� 4min��C��H2SO4��=$\frac{\frac{0.1mol}{0.1L}}{4min}$=0.25 mol/��L��min����
���ں�4min����H2SO4��ʾ��ƽ����Ӧ������ 0.25 mol/��L��min����
��3������ͬһ��Ӧ��ͬһʱ������У������ʵķ�Ӧ����֮�ȵ��ڼ�����֮�ȣ�����ǰ�������ڣ������ƽ����Ӧ����Ϊ0.25mol/��L��min��������4minʱ�������ƽ����Ӧ����Ϊ0.25 mol/��L��min����
����ǰ�������ڷ�Ӧ����һ���죬ԭ���ǣ���4������Һ��������Ũ����Ȼ��С�������ŷ�Ӧ���У���Һ�¶����ߣ���Ӧ�ӿ죬���·�Ӧ����ǰ��һ���죮
��ǰ2min���4min��ȣ���Ӧ����һ���죬��4������Һ��������Ũ����Ȼ��С�������ŷ�Ӧ���У���Һ�¶����ߣ���Ӧ�ӿ죬���·�Ӧ����ǰ��һ���죮
���� ������ע����ǣ������ַ�Ӧ���������֪��һ��Ҫ���й������㣬��ʵ������ʱ��Ҫ�Բ�������Ϊ�����м��㣬��Ŀ�Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
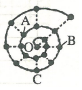 С�����о�Ԫ��ʱ���֣����Խ�ǰ18��Ԫ���ų���ͼ��ʾ�ġ���ţ����״��ͼ��ÿ����•������һ��Ԫ�أ�����O�������Ԫ�أ�����˵���д�����ǣ�������
С�����о�Ԫ��ʱ���֣����Խ�ǰ18��Ԫ���ų���ͼ��ʾ�ġ���ţ����״��ͼ��ÿ����•������һ��Ԫ�أ�����O�������Ԫ�أ�����˵���д�����ǣ�������| A�� | ����������Ԫ�ش���ͬһ�壬AԪ��λ��Ԫ�����ڱ���A�� | |
| B�� | ��O��ԽԶ��Ԫ��ԭ�Ӱ뾶һ��Խ�� | |
| C�� | B��C����������ˮ����������Ӧ | |
| D�� | BԪ����ͼ�н�������ǿ��Ԫ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������轺������Ҫ��ѧ�ɷֶ��Ƕ������� | |
| B�� | �ֻ����������̼��ά��Ĥ��һ���������ǽ������� | |
| C�� | �õ�����Һ����ֱ�Ӽ��麣ˮ���Ƿ�Ԫ�� | |
| D�� | ������ˮ��ԭ���͡�84������Һ������ԭ����ͬ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
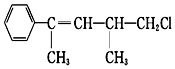
| A�� | �ڼ��Ⱥʹ��������£��������4 mol H2��Ӧ | |
| B�� | ��ʹ��ˮ��ɫ | |
| C�� | ����ʹKMnO4������Һ��ɫ | |
| D�� | һ�������£��ܷ���ȡ����Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��Ȳ���ģ�ͣ� | B�� | ������Ϊ��37��ԭ��${\;}_{37}^{17}$Cl | ||
| C�� | �Ȼ�þ����ʽ�� | D�� | �����ӵĽṹʾ��ͼ��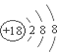 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | O3��O2�ȶ� | |
| B�� | O2��O3���������ֺ��أ�����ͬ�������� | |
| C�� | O2��O3���ת���ǻ�ѧ�仯 | |
| D�� | �ڱ�״���£��������O2��O3������ͬ��Ŀ����ԭ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | FeCl3 | B�� | CuS | C�� | HCl | D�� | Fe3O4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ͬһ�����Ԫ�ش��ϵ��½��������� | |
| B�� | Ԫ�����ڱ���Ԫ�������ɵľ��������ʽ | |
| C�� | ͬһ���ڴ����ң�Ԫ��ԭ�Ӱ뾶������ | |
| D�� | �ǽ���Ԫ�ص���������ϼ۵������ĸ����ϼ۵ľ���ֵ |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com