
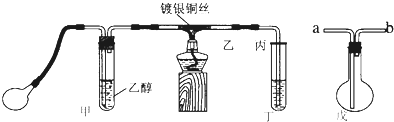
���� ��1�������¶��ܴٽ��Ҵ��Ļӷ���
��3���÷�Ӧ����������ȼ��ɽ��У�˵����Ӧ�Ƿ��ȵģ��Ҵ�����������������ȩ��
��4�����ݼ��е�λʱ���ڵ��������������������������ٶȹ��죬���߹������������Ա�֤��Ӧ�����¶ȣ��������ٶȹ��������Ĵ�������Ӧ����̫�٣��ﲻ����Ӧ�����¶ȷ�Ӧֹͣ��
��5����ȫƿ�еĵ����ǡ��̽���������
��� �⣺��1���Ҵ����лӷ��ԣ������¶��ܴٽ��Ҵ��Ļӷ���ʹ�����Ҵ����������ʼӿ죬���ƽ�ȵ��Ҵ�������
�ʴ�Ϊ���ʵ��ӿ������Ҵ����������ʣ����ƽ�ȵ��Ҵ�����
��3��ʵ��ʱ���ȼ��Ȳ��������еĶ�����˿��Լ1���Ӻ�����������ʱͭ˿���ʺ���״̬�����Ѿƾ��Ƴ��ߣ�����һ���Ĺ����ٶȣ�ͭ˿�ܳ�ʱ�䱣�ֺ���ֱ��ʵ�������˵����Ӧ����������ȼ��ɽ��е��ף�˵���÷�Ӧ�Ƿ��ȵķ�Ӧ���Ҵ�����������������ȩ��ˮ������ʽΪ��2CH3CH2OH+O2$��_{��}^{ͭ}$2CH3CHO+2H2O��
�ʴ�Ϊ�����ȣ�2CH3CH2OH+O2$��_{��}^{ͭ}$2CH3CHO+2H2O��
��4�����е�λʱ���ڵ�������Խ�࣬�����ٶ�Խ��֮ԽС���������ٶȹ�����������������߹������������Ա�֤��Ӧ�����¶ȣ����·�Ӧֹͣ���������ٶȹ�����Ӧ����̫�٣����ܴﵽ��Ӧ��Ҫ�¶ȣ�
�ʴ�Ϊ���ٿ��Ƽ��е�λʱ�������������ڴ��߹������������Ա�֤��Ӧ�����¶ȣ��۷�Ӧ����̫�٣����ܴﵽ��Ӧ��Ҫ�¶ȣ�
��5��Ϊ��ֹ��ֹ����ˮ��������ȫƿ�еĵ������ǡ��̽��������������ҽ�b��a�ӣ�
�ʴ�Ϊ��b��a��
���� ���⿼�����Ҵ��Ĵ�����ʵ�飬�����Ҵ��Ļ�ѧ�����Լ��Ҵ��Ĵ�����ʵ�����ʱ���Ĺؼ�����Ŀ�Ѷ��еȣ�


 �����ѧСѧ�꼶�νӽݾ��㽭��ѧ������ϵ�д�
�����ѧСѧ�꼶�νӽݾ��㽭��ѧ������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����ʺ���������һ����������ȫȼ�ն�ֻ����CO2��ˮ | |
| B�� | 75%��������������Ҵ���Һ������ҽ������ | |
| C�� | ʯ�͵ķ����ú�ĸ�������������仯 | |
| D�� | ��ϩ�ͱ�����ʹ��ˮ��ɫ����ɫ��ԭ����ͬ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
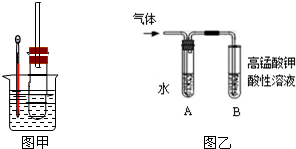 ����ͼʵ��װ�ã�����̨���ƾ����ԣ� ��֤����������ʣ�
����ͼʵ��װ�ã�����̨���ƾ����ԣ� ��֤����������ʣ��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
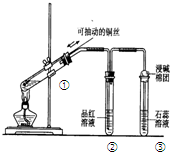
| A�� | �����ƶ�����ͭ˿�ɿ���SO2���� | |
| B�� | ����Ʒ����Һ����ɫ | |
| C�� | ����ʯ����Һ����ɫ | |
| D�� | Ϊȷ��CuSO4���ɣ�����м�ˮ���۲���Һ��ɫ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 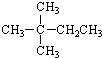 | B�� |  | C�� | CH3CH2CH2CH2CH3 | D�� | CH3CH2CH2CH3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
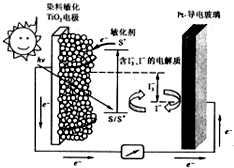 ��ͼ��һ��Ⱦ������̫���ܵ�ص�ʾ��ͼ����ص�һ���㼫���л�����ȼ�ϣ�S��Ϳ����TiO2����������Ƴɣ���һ�缫�ɵ��粣���Ʋ����ɣ�����з����ķ�ӦΪ��
��ͼ��һ��Ⱦ������̫���ܵ�ص�ʾ��ͼ����ص�һ���㼫���л�����ȼ�ϣ�S��Ϳ����TiO2����������Ƴɣ���һ�缫�ɵ��粣���Ʋ����ɣ�����з����ķ�ӦΪ��| A�� | ��ع���ʱ���ǽ�̫����ת��Ϊ���� | |
| B�� | ����жƲ����粣��Ϊ���� | |
| C�� | ��ع���ʱ��I-�����ڶƲ����粣���缫�Ϸŵ� | |
| D�� | ��صĵ������Һ��I-��I3-��Ũ�Ȳ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | v ��NO��=0.0010 mol•L-1•s-1 | B�� | v ��O2��=0.0010 mol•L-1•s-1 | ||
| C�� | v ��NH3��=0.010 mol•L-1•s-1 | D�� | v ��H2O��=0.045 mol•L-1•s-1 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com