
【题目】为探究影响化学反应速率的因素:在25mL 5%的H2O2溶液中,如表格中条件,产生等体积氧气时,所消耗时间最短的是:
组别 | V(1mol/L FeCl3)/mL | 蒸馏水/mL | 温度/℃ |
A | 2 | 2 | 50 |
B | 3 | 1 | 40 |
C | 2 | 2 | 40 |
D | 3 | 1 | 50 |
A.AB.BC.CD.D
 孟建平错题本系列答案
孟建平错题本系列答案 超能学典应用题题卡系列答案
超能学典应用题题卡系列答案科目:高中化学 来源: 题型:
【题目】用酸性甲醛燃料电池为电源进行电解的实验装置如图所示,下列说法中正确的是

A. 当a、b都是铜作电极时,电解的总反应方程式为2CuSO4+2H2O![]() 2H2SO4+2Cu+O2↑
2H2SO4+2Cu+O2↑
B. 燃料电池工作时,正极反应为O2+2H2O+4e-===4OH-
C. 当燃料电池消耗22.4 L甲醛气体时,电路中理论上转移2 mol e-
D. 燃料电池工作时,负极反应为HCHO+H2O-2e-===HCOOH+2H+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家对一碳化学进行了广泛深入的研究并取得了一些重要成果。
(1)已知:CO(g)+2H2(g)![]() CH3OH(g) ΔH1=-90.1kJ·mol-1;
CH3OH(g) ΔH1=-90.1kJ·mol-1;
3CH3OH(g)![]() CH3CH=CH2(g)+3H2O(g) ΔH2=-31.0 kJ·mol-1。
CH3CH=CH2(g)+3H2O(g) ΔH2=-31.0 kJ·mol-1。
CO与H2合成CH3CH=CH2的热化学方程式为______________________________________。
(2)现向三个体积均为2L的恒容密闭容器Ⅰ、Ⅱ、Ⅲ中,均分别充入1molCO和2molH2,发生反应:CO(g)+2H2(g)![]() CH3OH(g) ΔH=-90.1kJ·mol-1。三个容器的反应温度分别为T1、T2、T3且恒定不变。当反应均进行到5min时H2的体积分数如图1所示,其中只有一个容器中的反应已经达到平衡状态。
CH3OH(g) ΔH=-90.1kJ·mol-1。三个容器的反应温度分别为T1、T2、T3且恒定不变。当反应均进行到5min时H2的体积分数如图1所示,其中只有一个容器中的反应已经达到平衡状态。
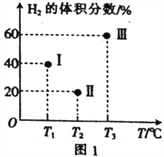
①5min时三个容器中的反应达到化学平衡状态的是容器_____________(填序号)。
②0~5min内容器Ⅰ中用CH3OH表示的化学反应速率v(CH3OH)=_________________。
③当三个容器中的反应均达到平衡状态时,CO的转化率最高的是容器____________(填序号,下同);平衡常数最小的是容器____________________。
(3)CO常用于工业冶炼金属,在不同温度下用CO还原四种金属氧化物,达到平衡后气体中lg![]() 与温度(T)的关系如图2所示。下列说法正确的是_____________(填字母)。
与温度(T)的关系如图2所示。下列说法正确的是_____________(填字母)。
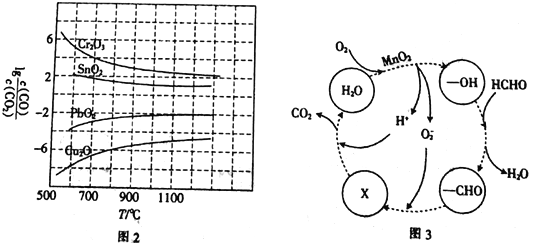
a.工业上可以通过增高反应装置来延长矿石和CO接触的时间,减少尾气中CO的含量
b.CO用于工业冶炼金属铬(Cr)时,还原效率不高
c.工业冶炼金属铜(Cu)时,600℃下CO的利用率比100℃下CO的利用率更大
d.CO还原PbO2反应的ΔH>0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数,下列说有关说法正确的是
A. 在常温常压下,11.2L N2含有的分子数小于0.5NA
B. 标准状况下,2.24L SO3含有的原子数为0.4NA
C. 将1L 2mol/L的FeCl3溶液,其中含有Cl-为2NA
D. 46g NO2和N2O4混合气体所含氧原子数目有可能为3NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2012年2月27日,昆明市一居民房因液化气泄漏引发火灾。已知液化气的主要成分是丙烷,下列有关丙烷的叙述不正确的是( )
A. 是直链烃,但分子中碳原子不在一条直线上
B. 在光照条件下能够与氯气发生取代反应
C. 丙烷比丁烷易汽化
D. 1 mol丙烷完全燃烧消耗5 mol O2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】烯烃与溴化氢、水加成时,产物有主次之分,例如:
![]()

下列框图中B、C、D都是相关反应中的主要产物(部分条件、试剂被省略),且化合物B中仅有4个碳原子、1个溴原子、1种氢原子。

上述框图中,B的结构简式为________;属于取代反应的有__________(填框图中序号),属于消去反应的有__________(填序号);写出反应④的化学方程式(只写主要产物,标明反应条件):__________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关下图中有机物的说法不正确的是
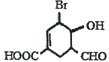
A. 该有机物的分子式为C8H9O4Br
B. 1mol该有机物最多可以与3molH2反应
C. 能发生酯化反应、水解反应、银镜反应和缩聚反应
D. 1mol该有机物与NaOH溶液反应时,最多消耗2molNaOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质的分类合理的是( )
A.酸性氧化物:SO2、SO3、CO2、CO
B.碱:烧碱、纯碱、苛性钾、氢氧化钡
C.混合物:铝热剂、漂白粉、水煤气、氢氧化铁胶体
D.电解质:稀硫酸、氢氧化钠、氯化钠、MgO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学实验室需要480mL,0.5mol/L的稀硫酸,现欲用98%的浓硫酸(ρ=1.84g/cm3 )配制,配制步骤包括:①计算所用浓硫酸的体积②转移③定容、上下颠倒摇匀④量取一定体积的浓硫酸⑤洗涤并转移⑥稀释并冷却至室温⑦轻摇混匀。完成下列问题:
(1)正确的操作顺序为(填入序号)________。选用的主要仪器有:量筒、烧杯、玻璃棒、________、________。
(2)应量取浓硫酸的体积为________;量取浓硫酸所用的量筒的规格是________(从下列中选用,填字母 A.10 mL B.25 mL C.50 mL D.100 mL);第⑥步中稀释实验的操作方法是________。
(3)下列关于容量瓶的使用方法中,正确的是________。
A.使用前要检验是否漏水
B.在容量瓶中直接溶解固体或稀释液体
C.溶液未经冷却即注入容量瓶中
D.向容量瓶中转移溶液要用玻璃棒引流
(4)下列情况中,所配制的稀硫酸浓度偏大的是________。
A.所用的浓硫酸长时间放置在密封不好的容器中
B.容量瓶用蒸馏水洗涤后残留有少量的水
C.所用过的烧杯、玻璃棒未洗涤
D.定容时俯视刻度线
E.用量筒量取浓硫酸时仰视刻度
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com