
| A. | ①②⑤ | B. | ①③④ | C. | ①②③⑤ | D. | ①③⑤ |
分析 ①元素的非金属性越强,其氢化物的稳定性越强;
②金属晶体的熔沸点与金属键成正比,金属键与电荷成正比、与半径成反比;
③第ⅠA、ⅡA族元素的阳离子与其上一周期稀有气体元素的原子具有相同的核外电子排布,但H元素除外;
④元素周期表中从ⅢB族到ⅡB族10个纵行的元素都是金属元素,为过渡元素;
⑤氢化物的熔沸点与其相对分子质量成正比,含有氢键的熔沸点较高.
解答 解:①元素的非金属性越强,其氢化物的稳定性越强,非金属性F>O>S,则氢化物的稳定性HF>H2O>H2S,故错误;
②金属晶体的熔沸点与金属键成正比,金属键与电荷成正比、与半径成反比,Na、K电荷相等,Al的电荷较大、半径大小为K>Na>Al,则熔点:Al>Na>K,故正确;
;
③第ⅠA、ⅡA族元素的阳离子与其上一周期稀有气体元素的原子具有相同的核外电子排布,但H元素除外,氢离子核外没有电子,故错误;
④元素周期表中从ⅢB族到ⅡB族10个纵行的元素都是金属元素,为过渡元素,故正确;
⑤氢化物的熔沸点与其相对分子质量成正比,含有氢键的熔沸点较高,氨气中含有氢键,则沸点:PH3<AsH3<NH3,故错误;
故选D.
点评 本题考查元素周期律,为高频考点,明确同一周期、同一主族元素原子结构和元素周期律关系是解本题关键,知道非金属性、金属性强弱比较方法,注意氢化物的熔沸点与氢键有关,题目难度不大.


 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 第四周期IA | B. | 第三周期0族 | C. | 第二周期VIIA | D. | 第三周期VIIA族 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1 mol Na2O2与足量CO2反应转移的电子数目为0.1 NA | |
| B. | 标准状况下,2.24 L CCl4中的分子数目为0.1 NA | |
| C. | 0.1 mol•L-1NaOH溶液中Na+的数目为0.1 NA | |
| D. | 3.2 g O2和O3的混合物含有的分子数目为0.1 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①④⑥⑦⑧ | B. | ②③④⑦⑧ | C. | ②③④⑥⑧ | D. | ③④⑤⑥⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
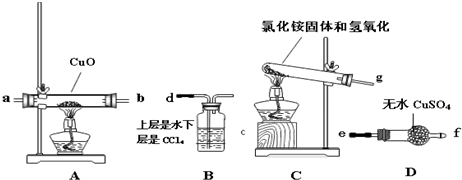
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加入BaCl2溶液,生成白色沉淀,加稀硝酸沉淀不消失,则原溶液中一定含SO42- | |
| B. | 用洁净的铂丝蘸取溶液在火焰上灼烧,产生黄色的火焰,则原溶液中一定不含K+ | |
| C. | 向某溶液中加入2滴KSCN溶液,溶液不显红色,再向溶液中滴几滴新制的氯水,溶液变为红色,该溶液中一定含有Fe2+ | |
| D. | 取少量晶体溶于水,加入少量NaOH溶液,加热,在试管口用湿润的蓝色石蕊试纸检验,若变红,则可证明晶体的成分中含有NH4+ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 升高温度,平衡常数增大 | |
| B. | 当v(CO2)正=$\frac{1}{2}$v(N2)逆时,说明反应达到平衡状态 | |
| C. | 增加CO的物质的量浓度,NO的转化率增大 | |
| D. | 增大压强,正反应速率增大,逆反应速率减小 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com