
| A. | 60ml 0.1mol/L的HCl溶液 | B. | 30ml 0.1mol/L的AlCl3溶液 | ||
| C. | 20ml 0.1mol/L的MgCl2溶液 | D. | 10ml 0.2mol/L的FeCl3溶液 |
 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案科目:高中化学 来源: 题型:选择题
| A. | 实验室制取氯气 MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O | |
| B. | 过量的氨水滴加到氯化铝溶液中 Al3++3NH3.H2O═Al(OH)3↓+3NH4+ | |
| C. | 氯气与水反应:Cl2+H2O═Cl-+H++HClO | |
| D. | 小苏打溶液中加入过量石灰水2HCO3-+Ca2++2OH-═CaCO3↓+CO32-+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 向FeCl3、CuCl2混合溶液中通入H2S和O2的混合气体可回收S,其转化关系如图.相关说法不正确的是( )
向FeCl3、CuCl2混合溶液中通入H2S和O2的混合气体可回收S,其转化关系如图.相关说法不正确的是( )| A. | 反应I的基本反应类型是复分解反应 | |
| B. | 反应II中每生成1molS需要2molFeCl3 | |
| C. | 在转化过程中能循环利用的物质有FeCl2和CuCl2 | |
| D. | 在转化过程中化合价不变的元素只有Cu和Cl |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | X和Y能形成共价化合物 | |
| B. | Y与W形成的化合物Y2W2中含有离子键和共价键 | |
| C. | 简单离子的半径:Y>Z>W>X | |
| D. | 最高价氧化物对应水化物的酸性:Z>W |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | pH=6的盐酸用水稀释100倍 | |
| B. | pH=10的氨水用水稀释100倍 | |
| C. | pH=10的氢氧化钠溶液稀释1000倍 | |
| D. | 0.1 mol•L-1的硫酸100 mL跟0.2 mol•L-1 NaOH溶液100 mL完全反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
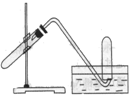
| A. | 加热NaHCO3制取和收集CO2 | |
| B. | 用铜和稀硝酸反应制取和收集NO | |
| C. | 用NH4Cl与浓NaOH溶液反应制取和收集NH3 | |
| D. | 用铜和浓硝酸反应制取和收集NO2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com