
A、B、C、D、E、F、G、H八种主族元素分布在三个不同的短周期,它们在周期表中位置如下:
A | ||||||
B | C[ | D | ||||
E | F | G | H | |||
请回答下列问题:
(1)写出E元素在周期表中的位置 。
(2)B与D可形成三原子分子X,X的电子式为 。
(3)E、F、H所形成的简单离子的半径由大到小的顺序为 (用离子符号表示)。
(4)G的最高价氧化物与B的单质在高温下能发生置换反应,其化学反应方程式为:
。
(5)由A、C、D三种元素组成的强电解质Z溶于水时能促进水的电离,测得Z的水溶液pH<7,其原因是 (用离子方程式来表示)。
(6)盐Y由B、D、E组成。以熔融盐Y为电解质构成的燃料电池如图所示。
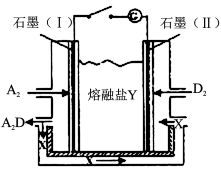
写出石墨(I)电极上发生的电极反应式 。
(7)用熔融盐Y的燃料电池作电源,以石墨为电极,电解一定浓度的CuSO 4 溶液至无色后继续电解一段时间。断开电路,向溶液中加入0.1 mol Cu(OH)2,溶液恢复到电解之前的体积和浓度,则电解过程中转移电子的物质的量为 。
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:2016届江西省赣州市十三县高三下期中理综化学试卷(解析版) 题型:实验题
[化学~选修2:化学与技术]
高炉炼铁的烟尘中主要含有锌、铁、铜等金属元素。从烟尘中提取硫酸锌,可以变废为宝,减少其对环境的危害。下图是用高炉烟尘制取硫酸锌的工业流程。
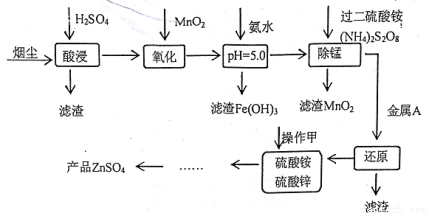
已知:①20℃时,0.1 mol.L-1的金属离子沉淀时的pH
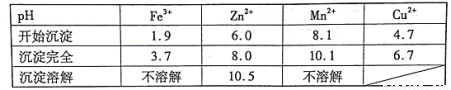
②过二硫酸铵是一种强氧化剂。
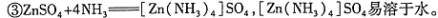
回答下列问题:
(1)为提高烟尘中金属离子的浸出率,除了适度增加硫酸浓度外,还可以采取什么措施?
(举出1种) 。
(2)上述流程测得溶液pH=5.0,此处可以选择的测量仪器是 。
(3)加入MnO2的目的是 。
(4)写出过二硫酸铵把硫酸锰(MnSO4)氧化的化学方程式 。
(5)写出还原过程发生的主要反应的离子方程式 。
(6)操作甲中为使锌离子完全沉淀,添加的最佳试剂是 。
A锌粉 B氨水 C( NH4)2CO3 D NaOH
(7)若pH=5.0时,溶液中的Cu2+尚未开始沉淀,求溶液中允许的Cu2+浓度的最大值
查看答案和解析>>
科目:高中化学 来源:2016届四川省邛崃市高三强化训练一化学试卷(解析版) 题型:选择题
已知KBiO3+MnSO4+H2SO4→Bi2(SO4)3+KMnO4+H2O+K2SO4(未配平),利用上述化学反应设计成如图所示原电池(盐桥中装有含琼胶的饱和K2SO4溶液),下列说法正确的是( )
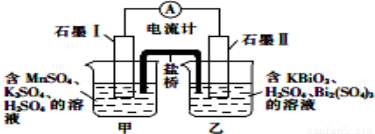
A.电池工作时,电子移向为石墨Ⅰ→溶液→盐桥→溶液→石墨Ⅱ
B.电池工作时,盐桥中的K+移向甲烧杯
C.甲烧杯中发生的电极反应为Mn2+﹣4e﹣+4H2O═MnO4﹣+8H+
D.电池工作一段时间后乙烧杯中溶液的pH增大
查看答案和解析>>
科目:高中化学 来源:2016届四川省宜宾县高三第一次适应性测试理综化学试卷(解析版) 题型:实验题
亚氯酸钠(NaClO2)是重要漂白剂,探究小组开展如下实验,请回答:
[实验Ⅰ]NaClO2晶体按如下图装置进行制取。
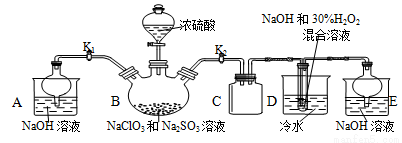
已知:NaClO2饱和溶液在低于38℃时析出NaClO2•3H2O,高于38℃时析出NaClO2,
高于60℃时NaClO2分解成NaClO3和NaCl。
(1)装置C起的是 的作用。
(2)已知装置B中的产物有ClO2气体,装置D中生成NaClO2和一种助燃气体,其反应的化学方程式为 。
(3)从装置D反应后的溶液中获得NaClO2晶体的操作步骤为:①减压在55℃蒸发结晶;
② ;③用38℃~60℃热水洗涤;④低于 ℃干燥;得到成品。.
(4)反应结束后,打开K1,装置A起的作用是 ;如果撤去D中的冷水浴,可能导致
产品中混有的杂质是 。
[实验Ⅱ]样品杂质分析与纯度测定
(5)测定样品中NaClO2的纯度:准确称一定质量的样品,加入适量蒸馏水和过量的KI晶体,在酸性条件下发生如下反应:ClO2﹣+4I﹣+4H+=2H2O+2I2+Cl﹣,将所得混合液稀释成100mL待测溶液。取25.00mL待测溶液,加入淀粉溶液做指示剂,用c mol•L﹣1 Na2S2O3标准液滴定至终点,测得消耗标准溶液体积的平均值为V mL(已知:I2+2S2O32﹣=2I﹣+S4O62﹣),则所称取的样品中NaClO2的物质的量为 。
查看答案和解析>>
科目:高中化学 来源:2016届四川省宜宾县高三第一次适应性测试理综化学试卷(解析版) 题型:选择题
NA为阿伏加德罗常数的值。下列说法中,正确的是( )
A.17 g甲基(-14CH3)所含电子数为10NA
B.标准状况下,0.56L丙烷中含有共价键的数目为0.2NA
C.在反应KClO3+6HCl=KCl+3Cl2↑+3H2O中,每生成3molCl2转移的电子数为5NA
D.0.1mol9038Sr原子中含中子数为3.8NA
查看答案和解析>>
科目:高中化学 来源:2016届天津市和平区高三第二次模拟考试化学试卷(解析版) 题型:选择题
下列说法正确的是( )。
A.C4H10有三种同分异构体
B.乙醇、乙二醇、丙三醇互为同系物,同系物之间不可能为同分异物体
C.常温下2S2O(g)=3S(s)+SO2(g)能自发进行,可推断该反应为放热反应
D.因为合金在潮湿的空气中易形成原电池,所以合金耐腐蚀性都较差
查看答案和解析>>
科目:高中化学 来源:2016届宁夏银川市高三4月质检理综化学试卷(解析版) 题型:实验题
黄铜矿(主要成分为CuFeS2 ,S为-2价)是工业炼铜的主要原料,现有一种天然黄铜矿(含SiO2),为了测定该黄铜矿的纯度,设计了如下实验:
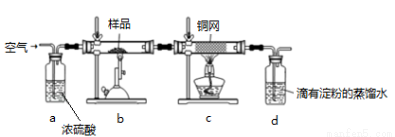
现称取研细的黄铜矿样品1.84g,在空气存在下进行煅烧,发生如下反应: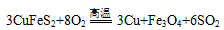
实验后取d中溶液的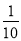 置于锥形瓶中,用0.0500mol/L标准碘溶液进行滴定,消耗标准溶液20.00mL。请回答下列问题:
置于锥形瓶中,用0.0500mol/L标准碘溶液进行滴定,消耗标准溶液20.00mL。请回答下列问题:
(1)中氧化产物是 ,当生成0.3molSO2气体时,转移电子 mol。
(2)将样品研细后再反应,其目的是 ;装置c的作用是 。
(3)用标准碘溶液滴定d中溶液的离子方程式是 ,滴定达终点时的现象是 。
(4)上述反应结束后,仍需通一段时间的空气,其目的是 。
(5)通过计算可知,该黄铜矿的纯度为 。
(6)若将原装置d中的试液换为Ba(OH)2溶液,测得黄铜矿纯度偏高,假设实验操作均正确,可能的原因主要是 。
查看答案和解析>>
科目:高中化学 来源:2016届山东省高三5月模拟一理综化学试卷(解析版) 题型:选择题
下列根据实验操作和现象所得出的结论不正确的是
选项 | 实验操作 | 实验现象 | 结论 |
A | 向某溶液中加入盐酸酸化的BaCl2溶液 | 有白色沉淀生成 | 溶液中不一定含有SO42- |
B | 向Fe(NO3)2溶液中滴入H2SO4酸化的H2O2溶液 | 溶液变为黄色 | 氧化性:H2O2﹥Fe3+ |
C | 将新制氯水和NaBr溶液在试管中混合后,加入CCl4,振荡静置 | 下层呈红棕色 | 氧化性:Cl2﹥Br2 |
D | 向0.1mol·L-1 AgNO3溶液中滴入稀盐酸至不再有沉淀产生,再滴加0.1mol·L-1 NaI溶液 | 先有白色沉淀后变为黄色沉淀 | Ksp:AgI<AgCl |
查看答案和解析>>
科目:高中化学 来源:2016届江苏省高三下学期考前练习化学试卷(解析版) 题型:选择题
下列有关化学用语正确的是
A.中子数为18的硫原子:3416S
B.氨分子的电子式: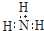
C.苯乙酸钠的结构简式: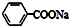
D.H2SO3的电离方程式:H2SO3?2H++SO32
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com