
在0.1 mol·L-1 CH3COOH溶液中存在如下电离平衡:CH3COOH  CH3COO-+H+对于该平衡,下列叙述正确的是
CH3COO-+H+对于该平衡,下列叙述正确的是
| A.加入水时,平衡向逆反应方向移动 |
| B.加入少量NaOH固体,平衡向正反应方向移动 |
| C.加入少量0.1 mol·L-1 HCl溶液,溶液中c(H+)减小 |
| D.加入少量CH3COONa固体,平衡向正反应方向移动 |
 文敬图书课时先锋系列答案
文敬图书课时先锋系列答案科目:高中化学 来源: 题型:单选题
常温时,将pH=3的H2SO4溶液和pH=12的NaOH溶液混合,当混合溶的
pH=10时,强酸和强碱的体积之比为( )
| A.1:9 | B.9:1 | C.10:1 | D.1:10 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
室温时,0.1 mol·L-1的HA 溶液的pH=3,向该溶液中逐滴加入NaOH,在滴加过程中,有关叙述正确的是
| A.原HA溶液中,c(H+)=c(OH-)+c(A-) |
| B.当滴入少量的NaOH,促进了HA的电离,溶液的pH降低 |
| C.当恰好完全中和时,溶液中c(Na+)>c(A-)>c(OH-)>c(H+) |
| D.当NaOH溶液过量时,可能出现:c(A-)>c(Na+)>c(OH-)>c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
25℃时,弱酸的电离平衡常数如下表:
| 弱酸 | CH3COOH | HCN | H2CO3 |
| Ka | 1.8×10-5 | 4.9×10-10 | K1:4.3×10-7 K2:5.6×10-11 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列有关电解质溶液中微粒浓度关系不正确的是
A.0.lmol/LpH=4的NaHA溶液中: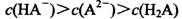 |
B.1mol/L的NaHCO3溶液中: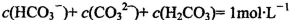 |
C.常温下,pH=7的NH4Cl与氨水的混合溶液中: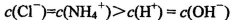 |
D.等体积、等物质的量浓度的NaX和弱酸HX的混合溶液中: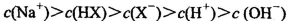 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
含有等物质的量NaOH的溶液分别用pH为2和3的CH3COOH溶液中和,设消耗CH3COOH溶液的体积依次为Va、Vb,则两者的关系正确的是( )
| A.Va>10 Vb | B.Va ="10" Vb |
| C.Vb >10 Va | D.Vb <10 Va |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
已知温度T时,水的离子积常数为KW,该温度下将V1mL a mol/L的一元酸HA与V2mL b mol·L-1的一元碱BOH充分混合,下列判断一定正确的是
A.若V1a=V2b,稀释此混合溶液时,溶液中各离子浓度一定都发生变化
B.若pH( HA)+pH(BOH) =14,则V1=V2时,酸碱恰好完全中和
C.此混合液中: c( H+)+c(B+) ≤ c(OH一)+c(A一)
D.若混合溶液中。c(OH一) =√KWmol·L-1,则此溶液一定呈中性
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
已知NaHSO3显酸性,NaHCO3溶液显碱性,现有浓度为0.1mol/L的NaHSO3和NaHCO3两种溶液,两种溶液中各粒子的物质的量浓度存在下列关系(R表示S或C),其中正确的一组是( )
A.c(Na+)>c(HRO3-)>c(H+)>c(RO32-)>c(OH-)
B.c(Na+)+c(H+)=c(HRO3-)+c(RO32-)+c(OH-)
C.c(H+)+c(H2RO3)=c(RO32-)+c(OH-)
D.c(Na+)=c(HRO3-)+(H2RO3)+2c(RO32-)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com