
| A、K+、MnO4-、Na+、Cl- |
| B、K+、Na+、NO3-、CO32- |
| C、Na+、H+、NO3-、SO42- |
| D、Al3+、Na+、Cl-、SO42- |
科目:高中化学 来源: 题型:
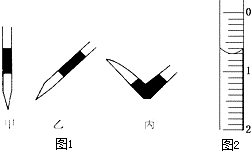 使用酸碱中和滴定法测定某未知物质的量浓度的稀盐酸.
使用酸碱中和滴定法测定某未知物质的量浓度的稀盐酸.滴定次数 实验数据/mL | 1 | 2 | 3 | 4 |
| V(样品) | 20.00 | 20.00 | 20.00 | 20.00 |
| V(NaOH)(消耗) | 15.80 | 15.00 | 15.02 | 14.98 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、钠的还原性很强,在空气中易变质,久置后变为过氧化钠 |
| B、氢氧化钠溶液可长时间保存在带磨口玻璃塞的试剂瓶中 |
| C、新制的氯水通常保存在棕色玻璃试剂瓶中,并现用现配 |
| D、漂粉精的有效成分为氯化钙 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、有紫黑色固体析出 |
| B、形成均匀的紫红色溶液 |
| C、液体分层,下层紫红色 |
| D、液体分层,上层紫红色 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| pH | c(CrO42-) | c(HCrO4-) | c(Cr2O72-) | c(H2CrO4) |
| 4 | 0.0003 | 0.1030 | 0.4480 | 0 |
| 6 | 0.0319 | 0.0899 | 0.4370 | 0 |
| 7 | 0.2645 | 0.0860 | 0.3195 | 0 |
| 9 | 0.8960 | 0.0031 | 0.0004 | 0 |
| A、铬酸的第一步电离方程式为:H2CrO4=H++HCrO4- |
| B、该铬酸溶液的物质的量浓度约为1.00mol/L |
| C、pH越大,HCrO4-越容易电离出CrO42- |
| D、NaHCrO4溶液中:c(OH-)>c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:
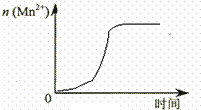 某化学小组为了研究外界条件对化学反应速率的影响,进行了如下实验:
某化学小组为了研究外界条件对化学反应速率的影响,进行了如下实验:| 实验编号 | 温度/℃ | 试管中所加试剂及其用量/mL | 溶液褪至无色所需时间/min | |||
| 0.6 mol/L H 2C2O4溶液 | H2O | 0.2 mol/L KMnO4溶液 | 3 mol/L 稀硫酸 | |||
| 1 | 20 | 3.0 | 2.0 | 3.0 | 2.0 | 4.0 |
| 2 | 20 | 3.0 | m | 2.5 | n | 4.8 |
| 3 | 20 | 3.0 | 3.0 | 2.0 | 2.0 | t1 |
| 4 | 30 | 3.0 | 2.0 | 3.0 | 2.0 | t2 |
| 实验编号 | 温度/℃ | 试管中所加试剂及其用量/mL | 再向试管中加入少量固体 | 溶液褪至无色所需时间/min | |||
| 0.6 mol/L H 2C2O4溶液 | H2O | 0.2 mol/L KMnO4溶液 | 3 mol/L 稀硫酸 | ||||
| 5 | 20 | 3.0 | 2.0 | 3.0 | 2.0 | t3 | |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、蒸发操作时,当出现大量晶体是,才能停止加热,用余热加热 |
| B、蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶的支管口处 |
| C、分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 |
| D、萃取操作时,应选择有机萃取剂,萃取剂的密度应比水大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
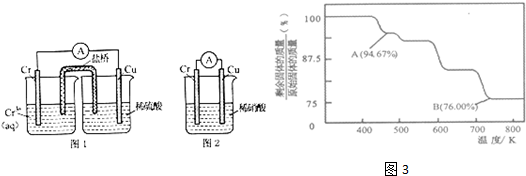
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com