
| 实验事实 | 结 论 | |
| ① | SO2使酸性高锰酸钾溶液褪色 | 可证SO2有漂白性 |
| ② | 用磨口玻璃瓶保存NaOH溶液,用热的纯碱溶液淸洗容器里附有的油污 | 都发生了氧化还原反应 |
| ③ | 取少量Na2SO3样品加入Ba(NO3)2溶液后,产生白色沉淀,滴加稀盐酸,沉淀不溶解 | 证明Na2SO3已氧化变质 |
| ④ | 某溶液加入稀盐酸产生能使澄清石灰水变浑浊的无色无味气体,该溶液滴加CaCl2溶液,有白色沉淀'生成 | 确定该溶液存在CO32- |
| ⑤ | 某无色溶液中加入浓氢氧化钠溶液并加热,产生的气体使湿润红色石蕊试纸变蓝 | 该溶液一定有NH4+ |
| A. | ①② | B. | ③④⑤ | C. | ②④ | D. | ④⑤ |
分析 ①SO2使酸性高锰酸钾溶液褪色,发生氧化还原反应;
②NaOH与二氧化硅反应,且纯碱利用油污的水解;
③Na2SO3样品加入Ba(NO3)2溶液后,生成亚硫酸钡,滴加稀盐酸,在酸性条件下发生氧化还原反应生成硫酸钡;
④气体为二氧化碳,且与氯化钙反应生成白色沉淀;
⑤氨气使湿润红色石蕊试纸变蓝.
解答 解:①SO2使酸性高锰酸钾溶液褪色,发生氧化还原反应,与还原性有关,与漂白性无关,故错误;
②NaOH与二氧化硅反应,且纯碱利用油污的水解,与氧化还原反应无关,故错误;
③Na2SO3样品加入Ba(NO3)2溶液后,生成亚硫酸钡,滴加稀盐酸,在酸性条件下发生氧化还原反应生成硫酸钡,不能说明是否变质,故错误;
④气体为二氧化碳,且与氯化钙反应生成白色沉淀,则确定该溶液存在CO32-,故正确;
⑤氨气使湿润红色石蕊试纸变蓝,则该溶液一定有NH4+,故正确;
故选D.
点评 本题考查化学实验方案的评价,为高频考点,把握物质的性质、发生的反应与现象、离子检验等为解答关键,侧重分析与实验能力的考查,注意实验的评价性分析,题目难度不大.


科目:高中化学 来源: 题型:解答题
 为维持人体血液中的血糖含量,在给病人输液时,通常用葡萄糖注射液,如图为病人输液用的葡萄糖(化学式为C6H12O6)注射液标签上的部分內容(该注射液就是葡萄糖的水溶液).试根据标签上的有关数据回答下列问题:
为维持人体血液中的血糖含量,在给病人输液时,通常用葡萄糖注射液,如图为病人输液用的葡萄糖(化学式为C6H12O6)注射液标签上的部分內容(该注射液就是葡萄糖的水溶液).试根据标签上的有关数据回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH3OH的燃烧热为192.9kJ•mol-1 | |
| B. | 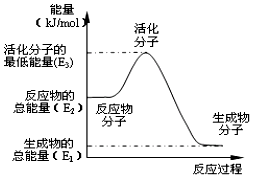 反应①中的能量变化如图所示,且△H1=E2-E1 | |
| C. | 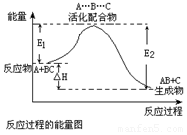 反应②中的能量变化如图所示,且△H2=E2-E1 | |
| D. | 根据②推知反应CH3OH(l)+$\frac{1}{2}$O2(g)═CO2(g)+2H2(g)△H>-192.9kJ•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 (1)将煤转化为水煤气是通过化学方法将煤转化为洁净燃料的方法之一.已知C(s)、CO(g)和H2(g)完全燃烧的热化学方程式分别为:
(1)将煤转化为水煤气是通过化学方法将煤转化为洁净燃料的方法之一.已知C(s)、CO(g)和H2(g)完全燃烧的热化学方程式分别为:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 检验方法 | 沉淀法 | 显色法 | 气体法 |
| 含义 | 反应中有沉淀产生或溶解 | 反应中有颜色变化 | 反应中有气体产生 |
| A. | NH4+-气体法 | B. | I--沉淀法 | ||
| C. | Na+-显色法 | D. | CO32--气体法和沉淀法 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 当 pH=7 时,若 V1=V2,则一定是 c2>c1 | |
| B. | 在任何情况下都满足 c(Na+ )+c(H+ )=c(CH3COO- )+c(OH- ) | |
| C. | 若 pH>7,则一定是 c1V1>c2V2 | |
| D. | 若 V1=V2,c1=c2,则 c(CH3COO-)+c(CH3COOH)=c(Na+) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 78g Na2O2与足量水充分反应时电子转移数为2NA | |
| B. | 25℃、101.3kPa时,11.2L H2中含有的原子数为NA | |
| C. | 4℃、101.3kPa时,54mL H2O中含有的分子数为3NA | |
| D. | 2L 1mol/L Na2SO4溶液中离子总数为3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CaO | B. | Ca(OH)2 | C. | SiO2 | D. | Al2O3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com