
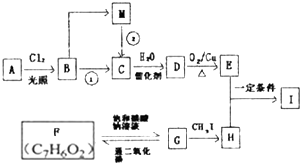
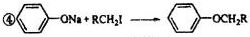
| 一定条件 |
 ,B转化得到C,C能与水反应得到D,D发生氧化反应得到E,则B在氢氧化钠醇溶液、加热条件下发生消去反应生成D,D与水发生加成反应生成D,且羟基连接氢原子较少的碳原子上,故C为
,B转化得到C,C能与水反应得到D,D发生氧化反应得到E,则B在氢氧化钠醇溶液、加热条件下发生消去反应生成D,D与水发生加成反应生成D,且羟基连接氢原子较少的碳原子上,故C为 ,D为
,D为 ,E为
,E为 .E的一种同分异构体可由M催化氧化得到,则M为
.E的一种同分异构体可由M催化氧化得到,则M为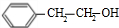 ,故B为
,故B为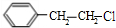 .
.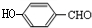 ,与饱和的碳酸钠溶液反应生成G为
,与饱和的碳酸钠溶液反应生成G为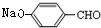 ,G与CH3I发生信息④中的取代反应生成H为
,G与CH3I发生信息④中的取代反应生成H为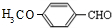 ,E与H发生信息⑤中反应生成生成I为
,E与H发生信息⑤中反应生成生成I为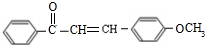 ,据此解答.
,据此解答. ,B转化得到C,C能与水反应得到D,D发生氧化反应得到E,则B在氢氧化钠醇溶液、加热条件下发生消去反应生成D,D与水发生加成反应生成D,且羟基连接氢原子较少的碳原子上,故C为
,B转化得到C,C能与水反应得到D,D发生氧化反应得到E,则B在氢氧化钠醇溶液、加热条件下发生消去反应生成D,D与水发生加成反应生成D,且羟基连接氢原子较少的碳原子上,故C为 ,D为
,D为 ,E为
,E为 .E的一种同分异构体可由M催化氧化得到,则M为
.E的一种同分异构体可由M催化氧化得到,则M为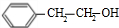 ,故B为
,故B为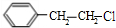 .
. ,与饱和的碳酸钠溶液反应生成G为
,与饱和的碳酸钠溶液反应生成G为 ,G与CH3I发生信息④中的取代反应生成H为
,G与CH3I发生信息④中的取代反应生成H为 ,E与H发生信息⑤中反应生成生成I为
,E与H发生信息⑤中反应生成生成I为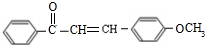 ,
, ,化学名称为乙苯,故答案为:乙苯;
,化学名称为乙苯,故答案为:乙苯; 与CH3I发生取代反应生成
与CH3I发生取代反应生成 ,由上述分析可知,I的结构简式为:
,由上述分析可知,I的结构简式为: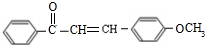 ,
,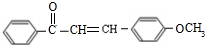 ;
; )的芳香同分异构体N既能发生银镜反应,又能发生水解反应,N为
)的芳香同分异构体N既能发生银镜反应,又能发生水解反应,N为 ,N在酸催化下发生水解反应的化学方程式为:
,N在酸催化下发生水解反应的化学方程式为: ,
, ;
; )的同分异构体中,既能发生银镜反应,又能与FeCl3溶液发生显色反应的共有13种,含有醛基、酚羟基,其中有5种不同化学环境的氢,其个数比为2:2:2:1:1的结构简式为
)的同分异构体中,既能发生银镜反应,又能与FeCl3溶液发生显色反应的共有13种,含有醛基、酚羟基,其中有5种不同化学环境的氢,其个数比为2:2:2:1:1的结构简式为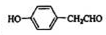 ,故答案为:
,故答案为: .
.


科目:高中化学 来源: 题型:
| A、0.2 | B、0.5 | C、1 | D、2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
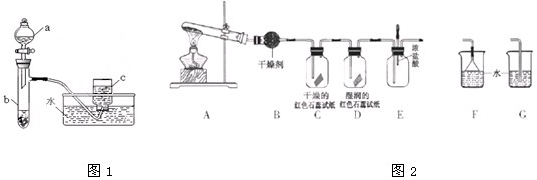
查看答案和解析>>
科目:高中化学 来源: 题型:
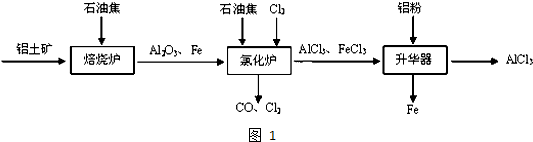
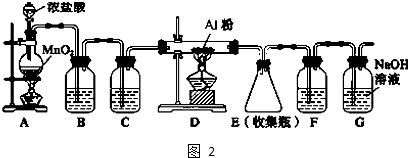
查看答案和解析>>
科目:高中化学 来源: 题型:
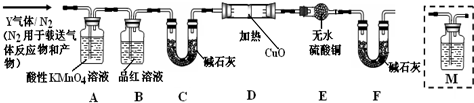
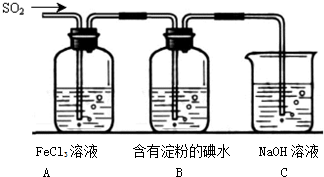
查看答案和解析>>
科目:高中化学 来源: 题型:
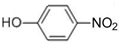 ⑥
⑥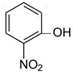 ⑦I2 ⑧H2O2 ⑨SiO2 ⑩NH4Cl
⑦I2 ⑧H2O2 ⑨SiO2 ⑩NH4Cl查看答案和解析>>
科目:高中化学 来源: 题型:
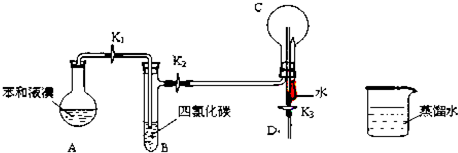
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、将钠投入硫酸铜溶液中只有紫红色固体析出 |
| B、过氧化钠投入硫酸亚铁溶液中出现白色沉淀 |
| C、氨水滴入氯化铝溶液中先出现白色沉淀后溶解 |
| D、饱和氯化钙溶液加入浓氢氧化钠溶液出现白色沉淀 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com